摘要:13.X.Y.Z三种主族元素的单质在常温下都是常见的无色气体.在适当条件下三者之间可以两两发生反应生成分别是双核.三核和四核的甲.乙.丙三种分子.且乙.丙分子中含有X元素的原子个数比为2∶3.请回答下列问题: (1)元素X的名称是 .丙分子的空间构型是 . (2)若甲与Y单质在常温下混合就有明显现象.则甲的化学式为 .丙在一定条件下转化为甲和乙的反应方程式为 . (3)①化合物丁含X.Y.Z三种元素.0.1 mol/L丁溶液的pH为1.将丁与丙按物质的量之比1∶1混合后所得物质戊的晶体结构中含有的化学键为 . a.只含共价键 b.只含离子键 c.既含离子键.又含共价键 ②常温下.戊的水溶液的pH 7(填“< “= 或“> ).其原因是 . 解析:X.Y.Z分别为H.O.N.甲.乙.丙分别为NO.H2O.NH3.NH3的空间构型为三角锥形.丁为HNO3.戊为NH4NO3.在NH4NO3晶体中既含离子键.又含极性共价键.NH4NO3水解显酸性. 答案:(1)氢 三角锥形 (2)NO 4NH3+5O24NO+6H2O (3)①c ②< NH+H2ONH3·H2O+H+
网址:http://m.1010jiajiao.com/timu3_id_84052[举报]
X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为2:3.请回答下列问题:
(1)元素X的名称是
(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为
(3)①化合物丁含X、Y、Z三种元素,0.1mol?L-1丁溶液的pH为1,将丁与丙按物质的量之比1:1混合后所得物质戊的结构中含有的化学键为
a.只含共价键
b.只含离子键
c.既含离子键,又含共价键
②常温下,戊的水溶液的pH
查看习题详情和答案>>
(1)元素X的名称是
氢
氢
.(2)若甲与Y单质在常温下混合就有明显现象,则甲的化学式为
NO
NO
.丙在一定条件下转化为甲和乙的反应方程式为4NH3+5O2
4NO+6H2O
| ||
| △ |
4NH3+5O2
4NO+6H2O
.
| ||
| △ |
(3)①化合物丁含X、Y、Z三种元素,0.1mol?L-1丁溶液的pH为1,将丁与丙按物质的量之比1:1混合后所得物质戊的结构中含有的化学键为
c
c
(选填序号).a.只含共价键
b.只含离子键
c.既含离子键,又含共价键
②常温下,戊的水溶液的pH
<
<
7 (填“<”、“=”或“>”),其原因是(用离子方程式表示)NH4++H2O?NH3?H2O+H+
NH4++H2O?NH3?H2O+H+
.X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如图1变化:一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
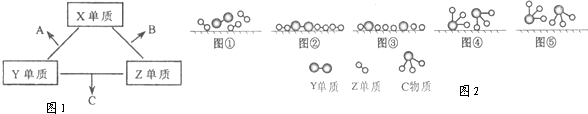
(1)X元素在周期表中的位置是 周期, 族.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们 .
(3)C的电子式是 ; Z单质与Y单质在固体催化剂表面合成C的反应过程,示意如图2.
图①至⑤中表示在催化剂表面Z单质与Y单质中化学键断裂是 .
(4)在一定条件下,1L密闭容器中充入1mol Y单质和3mol Z单质进行反应,经过20min达到平衡时,Y单质的物质的量为0.8mol,用题中所给数据列出平衡常数表达式(不必计算结果),K= ;用物质C表示该反应的反应速率为 .
(5)为幵发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料.写出由CO和Z单质在一定条件下生成甲醇的化学方程式 .用该反应合成1mol液态甲醇吸收热量131.9kJ,
又知:4H2(g)+2CO(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-1188.2kL/mol
H2O(g)=H2O(l)△H=-44.0kL/mol
请写出表达液态甲醇燃烧热的热化学方程式 .
查看习题详情和答案>>

(1)X元素在周期表中的位置是
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们
(3)C的电子式是
图①至⑤中表示在催化剂表面Z单质与Y单质中化学键断裂是
(4)在一定条件下,1L密闭容器中充入1mol Y单质和3mol Z单质进行反应,经过20min达到平衡时,Y单质的物质的量为0.8mol,用题中所给数据列出平衡常数表达式(不必计算结果),K=
(5)为幵发新能源,有关部门拟用甲醇(CH3OH)替代汽油作为公交车的燃料.写出由CO和Z单质在一定条件下生成甲醇的化学方程式
又知:4H2(g)+2CO(g)+3O2(g)=2CO2(g)+4H2O(g)△H=-1188.2kL/mol
H2O(g)=H2O(l)△H=-44.0kL/mol
请写出表达液态甲醇燃烧热的热化学方程式
(8分)X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10。请回答下列问题:
(1)X元素在周期表中的位置是 。
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在 。
(3)①C在一定条件下反应生成A的化学方程式是 。
②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐。该盐的水溶液pH<7,其原因是(写出离子方程式) 。
查看习题详情和答案>>
(8分)X、Y、Z三种短周期元素,它们的原子序数之和为16。X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
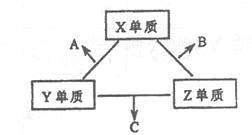
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10。请回答下列问题:
(1)X元素在周期表中的位置是 。
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在 。
(3)①C在一定条件下反应生成A的化学方程式是 。
②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐。该盐的水溶液pH<7,其原因是(写出离子方程式) 。
查看习题详情和答案>>
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)①C在一定条件下反应生成A的化学方程式是______.
②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐.该盐的水溶液pH______ 7(填“大于”、“小于”、“等于”),其原因是(写出离子方程式)______.
(4)已知Y单质与Z单质生成C的反应是可逆反应,△H<0.将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的有______.
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,C的体积分数增大.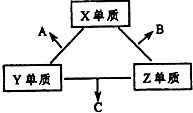
查看习题详情和答案>>
一个B分子中含有的Z原子个数比C分子中少1个,B、C两种分子中的电子数均等于10.请回答下列问题:
(1)X元素在周期表中的位置是______.
(2)分析同主族元素性质的递变规律,发现B、C物质沸点反常,这是因为它们的分子之间存在______.
(3)①C在一定条件下反应生成A的化学方程式是______.
②X、Y、Z三种元素可组成一种强酸W,C在适当条件下被W吸收生成一种盐.该盐的水溶液pH______ 7(填“大于”、“小于”、“等于”),其原因是(写出离子方程式)______.
(4)已知Y单质与Z单质生成C的反应是可逆反应,△H<0.将等物质的量的Y、Z两种单质充入一密闭容器中,在适当催化剂和恒温、恒压条件下反应.下列说法正确的有______.
a.达到化学平衡时,正反应速率与逆反应速率相等
b.反应过程中,Y单质的体积分数始终为50%
c.达到化学平衡时,Y、Z两种单质在混合气体中的物质的量之比为1:1
d.达到化学平衡的过程中气体平均相对分子质量减小
e.达到化学平衡后,升高温度,C的体积分数增大.
