网址:http://m.1010jiajiao.com/timu3_id_82545[举报]
(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流计。
锌片上发生的电极反应: ;
银片上发生的电极反应: 。
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
①产生氢气的体积(标准状况);
②通过导线的电量。(已知NA=6.02×1023/mol,电子电荷为1.60×10-19 C)
查看习题详情和答案>>|
已知0.1 mol/L邻苯二甲酸溶液的pH大于1,取等体积的邻苯二甲酸溶液和某KOH溶液混合,测得混合溶液的pH等于7,则碱与酸的浓度比值(x)为 | |
| [ ] | |
A. |
x>2 |
B. |
x=2 |
C. |
2>x>1 |
D. |
x=1 |
E. |
1>x> |
F. |
x= |
|
已知0.1 mol/L邻苯二甲酸溶液的pH大于1,取等体积的邻苯二甲酸溶液和某KOH溶液混合,测得混合溶液的pH等于7,则碱与酸的浓度比值(x)为 | |
| [ ] | |
A. |
x>2 |
B. |
x=2 |
C. |
2>x>1 |
D. |
x=1 |
E. |
1>x> |
F. |
x= |
(6分)氨在国民经济中占有重要的地位,请参与下列探究
(1)已知在400℃时,2NH3(g)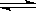 N2 (g)+ 3H2(g) (△H>0)的平衡常数K=2,
N2 (g)+ 3H2(g) (△H>0)的平衡常数K=2,
①400℃时,N2 (g)+ 3H2(g)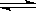 2NH3(g)的K= (填数值)。
2NH3(g)的K= (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应V(NH3)正 V(NH3)逆(填:>、<、=、不能确定)。
(2)已知: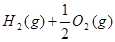 =H2O(l) △H=—285.8 kJ·
=H2O(l) △H=—285.8 kJ·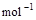 …①
…①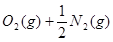 =NO2(g) △H=+33.9 kJ·
=NO2(g) △H=+33.9 kJ·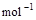 …②
…② 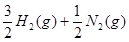 =NH3(g) △H=—46.0 kJ·
=NH3(g) △H=—46.0 kJ·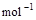 …③
…③
H2O(l)=H2O(g) △H=+44 kJ·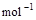 …④
…④
则表示NH3燃烧热的热化学方程式为