网址:http://m.1010jiajiao.com/timu3_id_80934[举报]
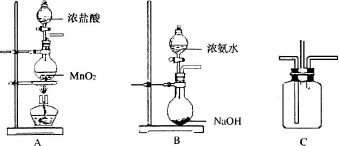
(12分)某校学生利用以下装置验证氯气与氨气之间的反应(部分装置已略去)。其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置A中发生反应的离子方程式为 。
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是 。
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为 。
(12分)某校学生利用以下装置验证氯气与氨气之间的反应(部分装置已略去)。其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置。


请回答下列问题:
(1)装置A中发生反应的离子方程式为 。
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是 。
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为 。
查看习题详情和答案>>
(12分)某校学生利用以下装置验证氯气与氨气之间的反应(部分装置已略去)。其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置A中发生反应的离子方程式为 。
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是 。
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为 。
查看习题详情和答案>>

请完成下列问题:
(1)装置A中发生反应的离子方程式为___________________________________________。
(2)装置B中浓氨水与NaOH固体混合可制取氨气,其原因是_______________________。
(3)装置C中氯气和氨气相遇,有浓厚的白烟并在容器内壁凝结,同时生成一种可参与生态循环的无毒气体,该反应的化学方程式为____________________________________,此反应可用于检查输送氯气的管道是否漏气。
(4)将装置C中反应生成的固体溶于水,所得溶液中离子浓度由大到小的顺序为__________。
查看习题详情和答案>>