摘要:(2010·安徽师大附中月考题)如图所示“合成氨 的演示实验.在Y形管的一侧用Zn粒和稀H2SO4反应制取H2.另一侧用NaNO2固体和 NH4Cl饱和溶液反应制取N2.N2和H2混合后通过还原铁粉来合成了NH3.再将产生的气体通入酚酞试液中.若酚酞试液变红.则说明产生了氨气. 某课外活动小组通过查阅资料和多次实验.得到了如下信息: 信息一:NaNO2固体和饱和NH4Cl溶液混合加热的过程中发生如下反应: ①NaNO2+NH4Cl===NH4NO2+NaCl ②NH4NO2===NH3+HNO2 ③2HNO2===N2O3+H2O ④2NH3+N2O3===2N2+3H2O 信息二:查阅资料.不同体积比的N2.H2混合气体在相同实验条件下合成氨.使酚酞试液变红所需要的时间如下: N2和H2的体积比,5∶1,3∶1,1∶1,1∶3,1∶5 酚酞变红色所需时间/min,8-9,7-8,6-7,3-4,9-10据此回答下列问题: (1)Y形管左侧管中发生反应的离子方程式 . (2)铁粉撒在石棉绒上的目的是 . (3)课外活动小组的同学们认为.该实验中即使酚酞变红也不能说明N2和H2反应合成了NH3.得出此结论的理由是 . 请你另设计一个简单的实验验证你的理由 . 欲解决这一问题.可以选用下图中的 装置连接在原装置中的 和 之间. (4)在上述实验过程中.为尽快观察到酚酞试液变红的实验现象.应该控制N2和H2:的体积比为 比较适宜,但该装置还难以实现此目的.原因是 . (5)实验过程中通入试管C中的气体成分有 . 解析:(1)根据Y形管右侧管需加热.说明右侧管反应制取N2.左侧管反应制取H2.(2)铁粉撒在石棉绒上的目的是增大与混合气体的接触面积.从而提高催化效率.增大反应速率.(3)因为NH4NO2分解可产生NH3.所以不能证明N2和H2反应生成了NH3. 答案:(1)Zn+2H+===Zn2++H2↑ (2)增大混合气体与催化剂的接触面积.使反应进行得更快 (3)从分步反应可知.产生N2的过程中.有可能直接产生氨气 将混合物加热产生的气体直接通入酚酞试液.若试液变红.则说明理由成立.否则.说明理由不成立 ③ A B (4)1∶3 无法控制通入B中N2和H2的体积比 (5)NH3.N2.H2
网址:http://m.1010jiajiao.com/timu3_id_80932[举报]
如图1所示“合成氨”的演示实验(夹持仪器均已省略).在Y形管的一侧用Zn粒和稀H2SO4反应制取H2,另一侧用NaNO2固体和NH4Cl饱和溶液反应制取N2,N2和H2混合后通过还原铁粉来合成NH3,再将产生的气体通入酚酞试液中,若酚酞试液变红,则说明产生了氨气.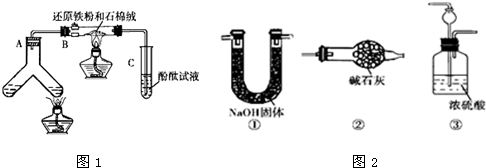
某课外活动小组通过查阅资料和多次实验,得到了如下信息:
信息一:NaNO2固体和饱和NH4Cl溶液混合加热的过程中发生如下反应:
①NaNO2+NH4Cl→NH4NO2+NaCl
②NH4NO2→NH3+HNO2
③2HNO2→N2O3+H2O
④2NH3+N2O3→2N2+3H2O
信息二:查阅资料,不同体积比的N2、H2 混合气体在相同实验条件下合成氨,使酚酞试液变红所需要的时间如下:
据此回答下列问题:
(1)Y形管左侧管中发生反应的离子方程式: .
(2)铁粉撒在石棉绒上的目的是 .
(3)课外活动小组的同学们认为,该实验中即使酚酞变红也不能说明N2和H2反应合成了NH3,得出此结论的理由是 ,请你另设计一个简单的实验验证你的理由 .欲解决这一问题,可以选用图2中的 装置连接在原装置中的 和 之间.
(4)在上述实验过程中,为尽快观察到酚酞试液变红的实验现象,应该控制N2和H2的体积比为 比较适宜;但该装置还难以实现此目的,原因是 .
(5)实验过程中通入试管C中的气体成分有 .
查看习题详情和答案>>

某课外活动小组通过查阅资料和多次实验,得到了如下信息:
信息一:NaNO2固体和饱和NH4Cl溶液混合加热的过程中发生如下反应:
①NaNO2+NH4Cl→NH4NO2+NaCl
②NH4NO2→NH3+HNO2
③2HNO2→N2O3+H2O
④2NH3+N2O3→2N2+3H2O
信息二:查阅资料,不同体积比的N2、H2 混合气体在相同实验条件下合成氨,使酚酞试液变红所需要的时间如下:
| N2和H2的体积比 | 5:1 | 3:1 | 1:1 | 1:3 | 1:5 |
| 酚酞变红色所需时间/min | 8~9 | 7~8 | 6~7 | 3~4 | 9~10 |
(1)Y形管左侧管中发生反应的离子方程式:
(2)铁粉撒在石棉绒上的目的是
(3)课外活动小组的同学们认为,该实验中即使酚酞变红也不能说明N2和H2反应合成了NH3,得出此结论的理由是
(4)在上述实验过程中,为尽快观察到酚酞试液变红的实验现象,应该控制N2和H2的体积比为
(5)实验过程中通入试管C中的气体成分有
下表各组物质中,物质之间不可能实现如图所示转化的是( )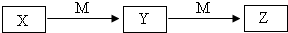
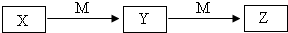
| 选项 | X | Y | Z | M |
| A | Fe | FeCl2 | FeCl3 | Cl2 |
| B | Mg | C | CO | CO2 |
| C | NaOH | Na2CO3 | NaHCO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A、A | B、B | C、C | D、D |
(2011?潍坊模拟)下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
|
查看习题详情和答案>>
化学是一门以实验为基础的科学,化学实验在化学学习中占有十分重要的地位,解答下列化学实验基本操作和技能题目.
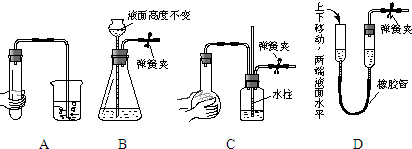
(1)如图所示装置的气密性检查中,漏气的是 .
(2)下列对实验仪器名称的标注或实验操作,正确的是 .
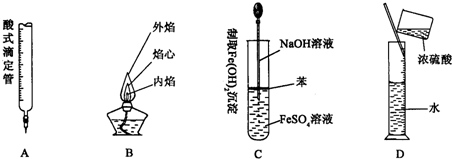
(3)下列说法中,完全正确的一组是 .
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过
的试管加热至沸腾
③等体积的浓氨水与蒸馏水混合后的溶液,其中氨水的溶质质量分数一定等于稀释前的一半
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤硝酸、溴水可长期盛放在棕色的滴瓶中
⑥将烧瓶放在桌上,再用力塞进塞子
⑦熔融氢氧化钠要在耐高温的石英坩埚中
⑧将滴管垂直伸进试管内滴加液体
A.①④B.①④⑤⑦C.②③⑤⑥D.①②③④⑤⑥⑦⑧ 查看习题详情和答案>>
(1)如图所示装置的气密性检查中,漏气的是

(2)下列对实验仪器名称的标注或实验操作,正确的是

(3)下列说法中,完全正确的一组是
①用试管夹夹持试管时,试管夹从试管底部往上套,夹在试管的中上部
②给盛有液体的体积超过
| 1 | 3 |
③等体积的浓氨水与蒸馏水混合后的溶液,其中氨水的溶质质量分数一定等于稀释前的一半
④将试管平放,用纸槽往试管里送入固体粉末后,然后竖立试管
⑤硝酸、溴水可长期盛放在棕色的滴瓶中
⑥将烧瓶放在桌上,再用力塞进塞子
⑦熔融氢氧化钠要在耐高温的石英坩埚中
⑧将滴管垂直伸进试管内滴加液体
A.①④B.①④⑤⑦C.②③⑤⑥D.①②③④⑤⑥⑦⑧ 查看习题详情和答案>>

 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )