摘要:17.短周期元素Q.R.T.W在元素周期表中的位置如下图所示.其中.T所处的周期序数与主族序数相等.请回答下列问题: (1)T的原子结构示意图为 . (2)元素的非金属性:Q W. (3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应.生成两种物质.其中一种是气体.反应的化学方程式为 . (4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物.此分解反应的化学方程式是 . (5)R有多种氧化物.其中甲的相对分子质量最小.在一定条件下.2 L的甲气体与0.5 L的氧气相混合.若该混合气体被足量的NaOH溶液完全吸收后没有气体残留.所生成R的含氧酸盐只有一种.则该含氧酸盐的化学式是 . (6)在298 K下.Q.T的单质各1 mol完全燃烧.分别放出热量a kJ和b kJ.又知一定条件下.T的单质能将Q从它的最高价氧化物中置换出来.若此置换反应生成3 mol Q的单质.则该反应在298 K下的ΔH= (注:题中所涉单质均为最稳定单质). 解析:由四种短周期元素在周期表中的位置可知T在第三周期.由于T所处的周期序数与主族序数相等.则T在ⅢA族为Al.则可推Q是C.R是N.W是S.(1)Al原子结构示意图为:.(2)由硫酸的酸性强于碳酸可知硫元素非金属性强于碳元素.即Q弱于W.(3)S单质与浓硫酸可发生氧化还原反应生成SO2气体.因为产物只有两种.产物中一定含H2O.则另一种为SO2.则反应化学方程式为:S+2H2SO4(浓)3SO2↑+2H2O.(4)比氮原子序数多1的元素是氧元素.其一种氢化物H2O2可分解生成它的另一种氢化物H2O.方程式为:2H2O22H2O+O2↑.(5)N的氧化物中相对分子质量最小的是NO.由反应方程式:2NO+O2===2NO2可知2 L NO与0.5 L O2混合后生成1 L NO2及余1 L NO.再由反应:NO+NO2+2NaOH===2NaNO2+H2O.混合气体被完全吸收后生成一种N的含氧酸盐为NaNO2.(6)由题目信息可知:4Al(s)+3O2(g)===2Al2O3(s),ΔH=-4b kJ/mol①.C(s)+O2(g)===CO2(g),ΔH=-a kJ/mol②.①-②×3可得:4Al(s)+3CO2(g)===2Al2O3,ΔH=(3a-4b) kJ/mol. 答案:(1) S+2H2SO4(浓)3SO2↑+2H2O (4)2H2O22H2O+O2↑ (5)NaNO2 (6)(3a-4b) kJ·mol-1
网址:http://m.1010jiajiao.com/timu3_id_79033[举报]
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
(1)T的原子结构示意图为


(2)元素的非金属性为(原子的得电子能力):Q
弱于
弱于
W(填“强于”或“弱于”).(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
S+2H2SO4(浓)
3SO2+2H2O
| ||
S+2H2SO4(浓)
3SO2+2H2O
.
| ||
(4)原子序数比R多1的元素的一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
2H2O2
O2↑+2H2O
| ||
2H2O2
O2↑+2H2O
.
| ||
(5)写出T、W两元素的最高价氧化物对应水化物相互反应时的离子方程式
Al(OH)3+3H+=Al3++3H2O
Al(OH)3+3H+=Al3++3H2O
.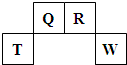 (2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.
(2009?福建)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等.请回答下列问题:
(1)T的原子结构示意图为


(2)元素的非金属性为(原子的得电子能力):Q
弱于
弱于
W(填“强于”或“弱于”).(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
S+2H2SO4(浓)
3SO2↑+2H2O
.
| ||
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
NaNO2
NaNO2
.(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ.又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的△H=
(3a-4b)kJ?mol-1
(3a-4b)kJ?mol-1
(注:题中所涉单质均为最稳定单质).短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与族序数相等,请回答下列问题:
(1)T的原子结构示意图为

(2)元素的原子的得电子能力为:Q
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为:
(4)原子序数比R多1的元素的一种氢化物在二氧化锰催化作用下易分解为它的另一种氢化物,此分解反应的化学方程式是
(5)将12gQ单质在足量的氧气中燃烧,所得气体通入1L1.5mol?L-1NaOH溶液中,完全吸收后,溶液中大量存在的离子有
查看习题详情和答案>>
| Q | R | ||
| T | W |


(2)元素的原子的得电子能力为:Q
<
<
W(填“>”或“<”).(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是具有漂白性的气体,反应的化学方程式为:
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
S+2H2SO4(浓)
3SO2↑+2H2O
| ||
(4)原子序数比R多1的元素的一种氢化物在二氧化锰催化作用下易分解为它的另一种氢化物,此分解反应的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
| ||
(5)将12gQ单质在足量的氧气中燃烧,所得气体通入1L1.5mol?L-1NaOH溶液中,完全吸收后,溶液中大量存在的离子有
Na+、HCO3-、CO32-
Na+、HCO3-、CO32-
. 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中元素T所处的周期序数与主族序数相等,请回答下列问题:(1)Q的最高价氧化物的电子式为


(2)元素的非金属性为:Q
弱于
弱于
W(填“强于”或“弱于”).(3)R的最高价氧化物的水化物的浓溶液能能与镁发生反应,其中R被还原到最低价,则反应的化学方程式为
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
.(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是
2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
.
| ||
(5)R有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是
NaNO2
NaNO2
. (2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )
(2013?番禺区模拟)短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列推断正确的是( )