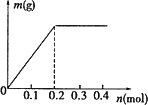
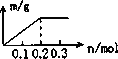摘要:4. 用Pt电极电解含有0.1 mol Cu2+和0.1 mol X3+的溶液.阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)的关系如图所示.则离子的氧化能力由大到小排列正确的是( ) A.Cu2+>X3+>H+ B.H+>X3+>Cu2+ C.X3+>H+>Cu2+ D.Cu2+>H+>X3+ 解析:有些同学没有认真分析.就将X3+与Fe3+联系起来.选择答案C.这其实是简单记忆阳离子放电顺序导致思维定势而造成的结果.本题的解题信息在图像中.一通电就有固体析出.且通过0.2 mol电子后.就没有固体析出了.说明是Cu2+放电的结果.X3+不放电.故正确答案为D. 答案:D
网址:http://m.1010jiajiao.com/timu3_id_78680[举报]
用Pt电极电解含有0.1 mol Cu2+和0.1 mol X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)的关系如图所示。则离子的氧化能力由大到小排列正确的是

[ ]
A.Cu2+>X3+>H+
B.H+>X3+>Cu2+
C.X3+>H+>Cu2+
D.Cu2+>H+>X3+
查看习题详情和答案>>
B.H+>X3+>Cu2+
C.X3+>H+>Cu2+
D.Cu2+>H+>X3+
用Pt电极电解含有各0.1 mol Cu2+和X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)的关系见下图。则离子的氧化能力由大到小排列正确的是( )
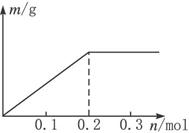
A.Cu2+>X3+>H+ B.H+>X3+>Cu2+
C.X3+>H+>Cu2+ D.Cu2+>H+>X3+
查看习题详情和答案>>|
用Pt电极电解含有Cu2+和X3+(X元素只有一种价态)均为0.1 mol的溶液,阴极析出金属的质量m(g)与溶液中通过电子的物质的量n(mol)关系如图,则离子的氧化能力由大到小排列正确的是
| |
| [ ] | |
A. |
Cu2+>X3+>H+ |
B. |
H+>X3+>Cu2+ |
C. |
X3+>H+>Cu2+ |
D. |
Cu2+>H+>X3+ |
|
用Pt电极电解含有各0.1 mol的Cu2-和X3+的溶液,阴极析出固体物质的质量m(g)与溶液中通过电子的物质的量n(mol)的关系见图示.
则离子的氧化能力由大到小排列正确的是: | |
| [ ] | |
A. |
Cu2+>X3+>H+ |
B. |
Cu2+>H+>X3+ |
C. |
X3+>H+>Cu2+ |
D. |
H+>X3+>Cu2+ |