网址:http://m.1010jiajiao.com/timu3_id_76588[举报]
(1)已知A的一种单质是一种重要的半导体材料,则A在元素周期表中的位置是
| ||
| ||
(2)X与纯碱高温熔融时能生成Z,同时还生成一种气体M;将一定量气体M通入z的水溶液中生成白色沉淀和纯碱溶液.X与纯碱高温熔融能发生反应的原因是
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(3)C的单质既可与盐酸、又可与NaOH溶液反应.一定条件下,Y和水作用生成含D的化合物W,W是一种含有10个电子的碱性气体.则Y的化学式是
(4)C的单质、石墨和二氧化钛(TiO2)按一定比例在高温下反应得到两种化合物,两种化合物均是由两种元素组成的新型陶瓷材料,则反应的化学方程式是(不必配平)
| ||
| ||
A元素的一种单质是一种重要的半导体材料,含A元素的一种化合物B可用于制造高性能的现代通讯材料——光导纤维,B与烧碱反应生成含A元素的化合物D。
(1)易与B发生化学反应的酸是________,(填化学名称)该化学反应的重要应用是__________________。
(2)将B与纯碱混合,高温熔融时也发生化学反应生成D,同时还生成氧化物C;
①写出生成D和C的化学反应方程式:
________________________________________________________________________
________________________________________________________________________。
②要将纯碱高温熔化,下列坩埚中不可选用的是________。
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
③将过量的C通入D的溶液中发生反应的化学方程式是:
________________________________________________________________________。
(3)B与石灰石、B与纯碱发生相似的化学反应。100 g B与石灰石的混合物充分反应后,生成的气体在标准状况下的体积为11.2 L,100 g混合物中石灰石的质量分数是________。
(4)A的单质与烧碱溶液和铝的单质与烧碱溶液发生相似的化学反应。相同物质的量的A的单质与铝的单质分别跟足量的烧碱溶液反应,生成的气体在同温同压下的体积之比为 。
查看习题详情和答案>>
化合物X由元素A、B组成,可用于制造高性能的现代通讯材料-光导纤维;化合物Y由不同短周期元素C、D组成,是良好的耐热、耐冲击材料.
(1)已知A的一种单质是一种重要的半导体材料,则A在元素周期表中的位置是______.A可由X与焦炭在高温下反应制得,其反应的化学方程式为______.
(2)X与纯碱高温熔融时能生成Z,同时还生成一种气体M;将一定量气体M通入z的水溶液中生成白色沉淀和纯碱溶液.X与纯碱高温熔融能发生反应的原因是______;M与Z的水溶液能发生反应的原因是______.要将纯碱高温熔化,下列坩埚中不可选用的是______.
A.普通玻璃坩埚 B.石英玻璃坩埚
C.氧化铝坩埚 D.铁坩埚
(3)C的单质既可与盐酸、又可与NaOH溶液反应.一定条件下,Y和水作用生成含D的化合物W,W是一种含有10个电子的碱性气体.则Y的化学式是______.
(4)C的单质、石墨和二氧化钛(TiO2)按一定比例在高温下反应得到两种化合物,两种化合物均是由两种元素组成的新型陶瓷材料,则反应的化学方程式是(不必配平)______.
查看习题详情和答案>>
物质A是由某元素组成的单质,将其在酒精灯火焰上灼烧,火焰为黄色,B.C.D是含A元素的三种不同化合物,E是一种气体单质,A.B.C.D按下图关系进行转化:
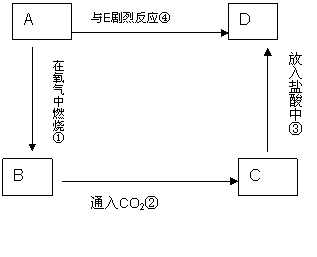 |
(1)写出化学式
A. B. D. E .
(2)上述反应属于氧化还原反应的是(填序号)
(3)画出A 的原子结构示意图
(4) 写出②③反应的化学方程式
②
③
查看习题详情和答案>>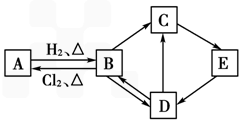
(2)A和B的互相转化在工业上有什么实际意义?__________。
(3)写出D→C反应的化学方程式:__________________________。
(4)写出E→D反应的化学方程式:__________________________。