网址:http://m.1010jiajiao.com/timu3_id_76446[举报]

(1)A装置中锥形瓶内装的某正盐固体是 ,分液漏斗中装的试剂是_________。
(2)B装置中所盛装的试剂是 ,该试剂的作用是_________________________。
(3)装置C中出现的现象是_______________________。
(4)通过上述实验可证明三种酸的酸性强弱顺序为__________________________。
查看习题详情和答案>> 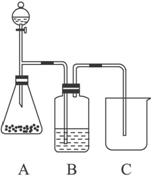
图15-9
(1)A装置中锥形瓶内装的某正盐固体是__________,分液漏斗中装的试剂是__________。
(2)B装置中所盛装的试剂是__________,该试剂的作用是_________________________。
(3)装置C中出现的现象是__________________________________________________。
(4)通过上述实验可证明三种酸的酸性强弱顺序为______________________________。
查看习题详情和答案>> 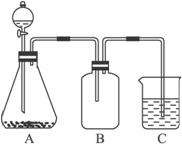
图6-19
(1)A装置中锥形瓶内装有某正盐固体是____________,分液漏斗中装的试剂是____________。
(2)B装置中所盛装的试剂是____________该试剂的作用是________________________。
(3)装置C中出现的现象是________________________。
(4)通过上述实验可证明三种酸的酸性强弱顺序为____________。
查看习题详情和答案>>为了确认CH3COOH、H2CO3和H2SiO3的酸性强弱,有人设计用下图所示装置,一次实验达到目的(不能再选用其他酸性溶液)。

(1)锥形瓶内盛放上面三种酸中的某种可溶性正盐固体,此固体为 ,分液漏斗中所盛试剂是 ;
(2)装置B中所盛试剂的名称是 ;装置B中所盛试剂的作用是 ;
(3)装置C中出现的现象是 。
查看习题详情和答案>>
| |||||||||||||||
