摘要:将70gNa2O2和Na2O的混合物跟98水充分反应后.所得NaOH溶液的质量分数为50%.计算原混合物中Na2O2和Na2O质量各为多少克?
网址:http://m.1010jiajiao.com/timu3_id_74185[举报]
将70gNa2O2和Na2O的混合物跟98g水充分反应后,所得NaOH溶液的质量分数为50%。
(1)分别写出Na2O2和Na2O跟水反应的化学方程式:________;________。
(2)计算原混合物中Na2O2和Na2O的物质的量分别是多少。
(3)若将上述溶液稀释至10L后,取出20mL该溶液用0.1mo1·L-1的H2SO4溶液中和。求需0.1mo1·L-1的H2SO4溶液的体积。
查看习题详情和答案>>
将70gNa2O2和Na2O的混合物跟98g水充分反应后,所得NaOH溶液的质量分数为50%。
(1)分别写出Na2O2和Na2O跟水反应的化学方程式:________;________。
(2)计算原混合物中Na2O2和Na2O的物质的量分别是多少。
(3)若将上述溶液稀释至10L后,取出20mL该溶液用0.1mo1·L-1的H2SO4溶液中和。求需0.1mo1·L-1的H2SO4溶液的体积。
查看习题详情和答案>>
 Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的
Ⅰ有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,A元素的原子是半径最小的原子.B元素的最高价氧化物的水化物与其氢化物反应生成一种盐X,D与A同族,且与E同周期,E元素的最外层电子数是次外层电子数的| 3 | 4 |
(1)写出相应元素符合,A
H
H
BN
N
CO
O
ES
S
(2)由A、C、D、E四种元素所组成的一种中学常见的化合物,它既能与盐酸反应,又能与NaOH溶液反应,在这种化合物的水溶液中,滴入紫色石蕊试液出现红色,则溶液中离子浓度由大到小的排列顺序为:
c(Na+)>c(HSO3-)>c(H+ )>c(SO32-)>c(OH-)
c(Na+)>c(HSO3-)>c(H+ )>c(SO32-)>c(OH-)
.(3)将铝片和镁片.插入由A、C、D三种元素组成物质的稀溶液中构成原电池,则负极的电极反应式为
2Al-6e-+8OH-=2AlO2-+4H2O
2Al-6e-+8OH-=2AlO2-+4H2O
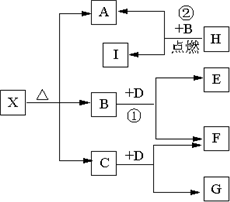
.Ⅱ(5分)已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有右图所示的关系.
试回答下列问题
(1)G的化学式为:
NaOH
NaOH
.(2)写出下列反应的化学方程式
①
2Na2O2+2CO2=2Na2CO3+O2
2Na2O2+2CO2=2Na2CO3+O2
②2Mg+CO2  2MgO+C
2MgO+C
 2MgO+C
2MgO+C2Mg+CO2  2MgO+C
2MgO+C
. 2MgO+C
2MgO+C下列实验操作中,正确的是( )
| A、除去乙酸乙酯中少量的乙酸,可用饱和碳酸钠溶液洗涤、分液 | B、白磷(P4)和Na都应保存在水中 | C、将铂丝用盐酸洗净后,在酒精灯的外焰上灼烧至没颜色,蘸取碳酸钾固体,再在酒精灯外焰灼烧,进行钾的焰色反应 | D、将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴滴入1~2mLFeCl3稀溶液.继续煮沸至溶液呈红褐色,停止加热,得到Fe(OH)3胶体 |