网址:http://m.1010jiajiao.com/timu3_id_72841[举报]
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C是一种重要的能源,C和K都是由极性键构成的非极性分子,J和E是工业上用途很广的重要化工原料,X为无色液体。(图中部分反应物或生成物没有列出)

请按要求回答:
(1)写出A的化学式 H的电子式
(2)反应①中每生成l mol F,转移电子的物质的量为
(3)反应②进行的条件为
(4)反应③的化学方程式为
(5)反应④的离子方程式为
查看习题详情和答案>>已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为无色液体.反应生成的水均已略去.它们有如下图所示的关系.

(1)写出化学式:A________ B________ J________.
(2)反应③中每生成1 mol F,转移电子的数目为:________.
(3)反应④的化学方程式为:________.
(4)写出离子方程式分别为:反应②________;⑤________.
(5)反应①中,每1.00 g C与足量的F作用,恢复到25℃放出55.6 kJ热量,写出反应①的热化学方程式 ________.
已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体.反应生成的水均已略去.它们有如下图所示的关系.

(1)写出化学式:A________,B________,J________.
(2)反应③中每生成1 mol F,转移电子的数目为________.
(3)反应④的化学方程式为:________.
(4)写出离子方程式:
反应②________;
反应⑤________.
(5)反应①中,每1.00 g C与足量的F作用,恢复到25℃放出55.6 kJ热量,写出反应①的热化学方程式________.
(8分)已知A、B均是由两种元素组成的化合物,A中某种元素的质量分数为75%,B是一种淡黄色固体,C、J是同周期元素的气态氢化物,其中C是含氢量最高的烃,X为常见的无色液体。反应生成的水均已略去。它们有如下图所示的关系。
(1)写出化学式:A________,B________,J________。
(2)反应③中每生成1 mol F,转移电子的数目为______________。
(3)反应④的化学方程式为:______________________________。
(4)写出离子方程式:
反应②_______________________________________________;
反应⑤________________________________________________。
(5)反应①中,每1.00 g C与足量的F作用,恢复到25 ℃放出55.6 kJ热量,写出
反应①的热化学方程式 。
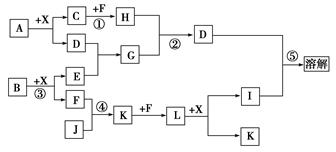
(1)写出化学式:A________,B________,J________。
(2)反应③中每生成1 mol F,转移电子的数目为______________。
(3)反应④的化学方程式为:______________________________。
(4)写出离子方程式:
反应②_______________________________________________;
反应⑤________________________________________________。
(5)反应①中,每1.00 g C与足量的F作用,恢复到25 ℃放出55.6 kJ热量,写出
反应①的热化学方程式 。