摘要:8.某溶液中含有Ba2+.Cu2+.Ag+.现用NaOH溶液.盐酸和Na2SO4溶液将这三种离子逐一沉淀分离.其流程如下图所示.下列说法正确的是( ). A.试剂A为Na2SO4溶液 B.沉淀3的化学式可能是BaSO4 C.生成沉淀1的离子方程式为:Cu2++2OH-=Cu(OH)2↓ D.生成沉淀2的离子方程式为:Ag++Cl-=AgCl↓ [解析]选B.含有Ba2+.Cu2+.Ag+的溶液中.若先加NaOH溶液.则会产生Cu(OH)2和AgOH(或Ag2O)两种沉淀,若先加Na2SO4溶液.则会产生BaSO4和Ag2SO4两种沉淀,若先加盐酸.则只会产生AgCl一种白色沉淀.所以试剂A为盐酸溶液.所得溶液1中含有Ba2+和Cu2+,若向溶液1中先加NaOH溶液.则只会产生Cu(OH)2沉淀.若先加Na2SO4溶液.则会产生BaSO4一种沉淀.所以NaOH溶液和Na2SO4溶液加入的先后顺序.对“离子逐一沉淀分离 的要求无影响.即B为NaOH溶液或Na2SO4溶液.沉淀2为Cu(OH)2或BaSO4沉淀.C为Na2SO4溶液或NaOH溶液.沉淀3为BaSO4或 Cu(OH)2沉淀.
网址:http://m.1010jiajiao.com/timu3_id_71706[举报]
某溶液中含有Ba2+、HCO3-、Cl-、NO3-四种离子,先向溶液中加入足量NaOH,再加入足量稀盐酸,溶液中大量减少的是( )
| A、Ba2+ | B、HCO3- | C、Cl- | D、NO3- |
某溶液中含有Ba2+、Cu2+ 和Ag+,现用氢氧化钠、盐酸和硫酸钠溶液将三种离子逐一沉淀分离。其流程如下图所示:(其中“溶液2”为无色溶液)
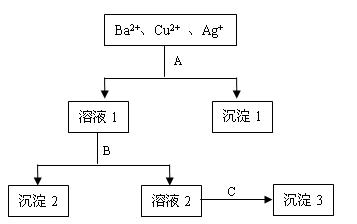
回答下列问题:
(1)沉淀1的化学式: 。
(2)写出下列反应的离子方程式:
溶液1 + B: 。
溶液2 + C: 。
查看习题详情和答案>>某溶液中含有Ba2+、Cu2+ 和Ag+,现用氢氧化钠、盐酸和硫酸钠溶液将三种离子逐一沉淀分离。其流程如下图所示:(其中“溶液2”为无色溶液)
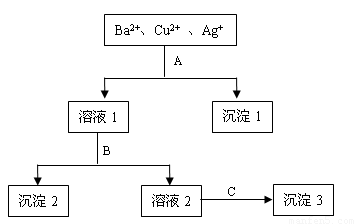
回答下列问题:
(1)沉淀1的化学式: 。
(2)写出下列反应的离子方程式:
溶液1 + B: 。
溶液2 + C: 。
查看习题详情和答案>>


 C: 。
C: 。