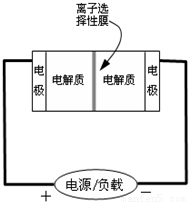
摘要:15.如图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐.中央为电池.电解质通过泵不断在储罐和电池间循环,电池中的左右两侧为电极.中间为离子选择性膜.在电池放电和充电时.该膜可允许钠离子通过,放电前.被膜隔开的电解质为Na2S2和NaBr3.放电后.分别变为Na2S4和NaBr.下列说法正确的是 A.电池充电时.阳极电极反应式为:3Br--2e-=Br3- B.电池放电时.负极电极反应方程式为:2S22-+2e-=S42- C.电池放电时.电池的总反应方程式为:Na2S4+3NaBr=2 Na2S2+ NaBr3 D.在充电过程中钠离子从右边通过离子选择性膜流向左边 第Ⅱ卷
网址:http://m.1010jiajiao.com/timu3_id_71441[举报]
 由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.
由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.Ⅰ.过硫化钠加入盐酸中有硫沉淀析出,写出该反应的化学方程式
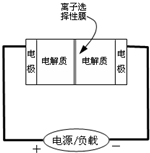
Ⅱ.某些多硫化钠可用于制作蓄电池.如图是一种正在投入生产的大型蓄电系统的原理图.放电充电
电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3
| 放电 | 充电 |
(1)电池中的左侧“电极”的电极名称是
(2)放电过程中钠离子从
(3)写出充电过程中阳极的电极反应式
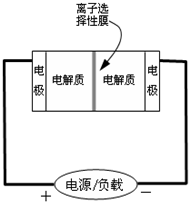 如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3
如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为:2Na2S2+NaBr3| 放电 |
| 充电 |
①充电的过程中当0.1molNa+通过离子交换膜时,导线通过0.1mol电子
②电池放电时,负极反应为:3NaBr-2e-=NaBr3+2Na+
③充电过程中钠离子从右到左通过离子交换膜
④放电过程中钠离子从右到左通过离子交换膜
上述关于此电池说法正确的是( )
查看习题详情和答案>>
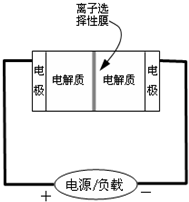
 (2009?揭阳二模)如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为2Na2S2+NaBr3
(2009?揭阳二模)如图是一种正在投入生产的大型蓄电系统的原理图.电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜只允许钠离子通过.电池充、放电的化学反应方程式为2Na2S2+NaBr3| 放电 |
| 充电 |
查看习题详情和答案>>
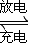 Na2S4+3NaBr
Na2S4+3NaBr