摘要:24.人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积 的血样.加适量的草酸铵[(NH4)2C2O4]溶液.可析出草酸钙(CaC2O4)沉淀.将 此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4).再用KMnO4溶液滴定即可测定 血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓 度: [配制KMnO4标准溶液]下图是配制50mLKMnO4标准溶液的过程示意图. (1)请你观察图示判断其中不正确的操作有 , (2)其中确定50mL溶液体积的容器是 , (3)如果按照图示的操作所配制的溶液进行实验.在其他操作均正确的情况下.所测得的实验结果将 [测定血液样品中Ca2+的浓度]抽取血样20.00mL.经过上述处理后得到草酸.再用0.020mol/LKMnO4溶液滴定.使草酸转化成CO2逸出.这时共消耗12.00mL KMnO4溶液. (4)已知草酸跟KMnO4反应的离子方程式为: 2MnO4―+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O 则式中的 . (5)滴定时.根据现象 .即可确定反应达到终点. (6)经过计算.血液样品中Ca2+离子的浓度为 mg/cm3. [解析](1)量筒不能用于配制溶液.视线应该与凹液面的最低点相平读数.所以②⑤操作错误,(2)配制50mL一定物质的量浓度KMnO4标准溶液需要50mL的容量瓶,(3)仰视读数时.定容时.所加的水超过刻度线.体积偏大.所以浓度偏小.血样处理过程中发生反应的离子方程式依次是:①Ca2++C2O42-=CaC2O4↓,②CaC2O4+2H+=Ca2++H2C2O4,③2MnO4―+5H2C2O4+6H+=2Mnx++10CO2↑+8H2O.由此可得如下关系式:5Ca2+-5CaC2O4-5H2C2O4-2MnO4―.所以n(Ca2+)=n(MnO4-)=×0.0120L ×0.020mol·L-1=6.0×10-4mol.血液样品中Ca2+的浓度==1.2×10-3g/cm3=1.2mg/cm3.对于反应③根据电荷守恒.2×=2×(+x).所以x=2.草酸溶液无色.当反应正好完全进行的时候.多加一滴KMnO4溶液.溶液恰好由无色变为紫红色. [答案]容量瓶 (3)偏小 溶液由无色变为紫红色 (6)1.2 () 来源: 版权所有:()
网址:http://m.1010jiajiao.com/timu3_id_71196[举报]
人体血液里Ca2+的浓度一般采用mg/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度.
配制KMnO4标准溶液如图所示是配制50mL KMnO4 标准溶液的过程示意图.

(1)请你观察图示判断,其中不正确的操作有(填序号)
(2)其中确定50mL溶液体积的容器是(填名称)
(3)如果用图示的操作配制溶液,所配制的溶液浓度将
测定血液样品中Ca2+的浓度:抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4 溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液.
(4)已知草酸跟KMnO4反应的离子方程式为:2MnO
+5H2C2O4+6H+═2Mnx++10CO2↑+8H2O
则方程式中的x=
(5)经过计算,血液样品中Ca2+的浓度为
查看习题详情和答案>>
配制KMnO4标准溶液如图所示是配制50mL KMnO4 标准溶液的过程示意图.

(1)请你观察图示判断,其中不正确的操作有(填序号)
②⑤
②⑤
;(2)其中确定50mL溶液体积的容器是(填名称)
容量瓶
容量瓶
;(3)如果用图示的操作配制溶液,所配制的溶液浓度将
偏小
偏小
(填“偏大”或“偏小”).测定血液样品中Ca2+的浓度:抽取血样20.00mL,经过上述处理后得到草酸,再用0.020mol/L KMnO4 溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL KMnO4溶液.
(4)已知草酸跟KMnO4反应的离子方程式为:2MnO
- 4 |
则方程式中的x=
2
2
.(5)经过计算,血液样品中Ca2+的浓度为
1.2
1.2
mg/cm3.人体血液里Ca2+的浓度一般采用g/cm3来表示(即1 cm3血样中含有的Ca2+的质量)。抽取 一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得弱酸草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度。某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度。
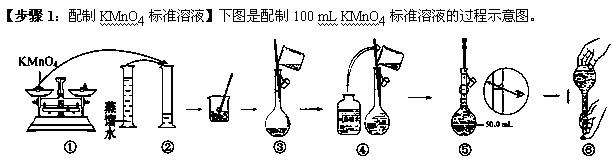 (1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(1)请你观察图示判断,其中不正确的两项操作有 (填序号);
(2)其中确定100 mL溶液体积的仪器是__________________
(3)如果用图示的操作所配制的溶液进行实验,在其他操作正确的情况下,所配制的溶液浓度将
______(填“偏大”或“偏小”)。
【步骤2:测定血液样品中Ca2+的浓度】抽取血样20.00 mL,经过上述处理后得到草酸,再用0.020 mol/L 酸性KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00 mL KMnO4溶液。
(4)写出草酸与酸性KMnO4溶液反应的离子方程式 。
(5)滴定的终点为 。
(6)经过计算,血液样品中Ca2+的浓度为__________g/cm3。
查看习题详情和答案>>(2011?泰州一模)缓冲溶液可以抗御少量酸碱对溶液pH的影响.人体血液里最主要的缓冲体系是碳酸氢盐缓冲体系(H2CO3/HCO3-),维持血液的pH保持稳定.己知在人体正常体温时,反应H2CO3?HCO3-+H+的Ka=10-6.1mol?L-1,正常血液中c(HCO3-):c(H2CO3)≈20:1,lg2=0.3,lg5=0.7.则下列判断正确的是( )
查看习题详情和答案>>
(2013?济宁一模)化学反应变化过程及结果的研究.按要求回答问题:(1)关于反应过程中能量变化的研究:

则:2CO(g)+O2(g)=2CO2(g)△H=
(2)关于反应速率和限度的研究:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+CO2 (g)?CO(NH2)2 (l)+H2O (l),该反应的平衡常数(K)和温度(T/℃)关系如下:
①焓变△H
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
=x,如图(1)是氨碳比(x)与CO2平衡转化率(α)的关系.α随着x增大而增大的原因是
③图(1)中的B点处,NH3的平衡转化率为
(3)关于电化学的研究:
铝是日常生活中用途最多的金属元素,如图(2)为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝电极反应式为

(4)关于电离平衡的研究:
CO2+H2O?H2CO3
HCO3-人体血液里存在重要的酸碱平衡:,使人体血液pH保持在7.35~7.45,否则就会发生酸中毒或碱中毒.其pH随c(HCO3-):c(H2CO3)变化关系如下表:
试回答:
①正常人体血液中,HCO3-的水解程度
②人体血液酸中毒时,可注射缓解
A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③pH=7.00的血液中,c(H2CO3)
查看习题详情和答案>>

则:2CO(g)+O2(g)=2CO2(g)△H=
-(a-2b+4c)
-(a-2b+4c)
kJ?mol-1.(2)关于反应速率和限度的研究:
工业生产尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为:
2NH3 (g)+CO2 (g)?CO(NH2)2 (l)+H2O (l),该反应的平衡常数(K)和温度(T/℃)关系如下:
| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
<
<
0 (填“>”、“<”或“=”).②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
| n(NH3) |
| n(CO2) |
c(NH3)增大,平衡正向移动
c(NH3)增大,平衡正向移动
.③图(1)中的B点处,NH3的平衡转化率为
32
32
%.(3)关于电化学的研究:
铝是日常生活中用途最多的金属元素,如图(2)为Al-AgO电池的构造简图,电解质溶液为NaOH,它可用作水下动力电源,该电池中铝电极反应式为
Al+4OH--3e-=AlO2-+2H2O
Al+4OH--3e-=AlO2-+2H2O
.用该电池电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图如图(3)(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极).电解时,阳极的电极反应式为CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O
CO(NH2)2+8OH--6e-=CO32-+N2↑+6H2O
.
(4)关于电离平衡的研究:
CO2+H2O?H2CO3
| OH- |
| H+ |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
①正常人体血液中,HCO3-的水解程度
大于
大于
电离程度(填“大于”、“小于”、“等于”);②人体血液酸中毒时,可注射缓解
B
B
(填选项);A.NaOH溶液 B.NaHCO3溶液 C.NaCl溶液 D.Na2SO4溶液
③pH=7.00的血液中,c(H2CO3)
<
<
c(HCO3-) (填“<”、“>”、“=”)