网址:http://m.1010jiajiao.com/timu3_id_6307[举报]
影响气体物质溶解度的因素除与溶质和溶剂性质有关外,还与______________、______________有关。20℃时,Cl2的溶解度为2.5,其意义是:在20℃时,压强为____________时,在____________水中,最多可溶解Cl2____________。
查看习题详情和答案>>影响气体物质溶解度的因素除与溶质和溶剂性质有关外,还与_____、_____有关。20℃时,Cl2的溶解度为2.5,其意义是:在20℃时,压强为______时,在________水中,最多可溶解Cl2________。
查看习题详情和答案>>(1)从组成角度看:水是由 ______组成的。
(2)从微粒角度看:水是由 ____ 构成的。
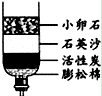
(3)从资源角度看:水是生命之源,下图是用来净化河水的简易装置, 下列说法错误的是 。
A.水是一种重要的溶剂
B.利用下图装置能把硬水变为软水
C.通过过滤可以除去水中所有的杂质
D.利用下图装置能对水杀菌消毒
①水通电分解生成最理想的能源-- 氢气,反应的化学方程式为 ;在电解水的实验中,若某个电极产生5 mL 气体时,则另一电极产生的气体体积可能是 ____ mL(不考虑其它因素的影响)。
②甲物质是一种重要的有机化工原料。一定质量的甲和48g乙按下图所示充分反应,当乙完全反应时,可生成44g丙和36g丁,则甲中所含各元素的质量比为 __ 。
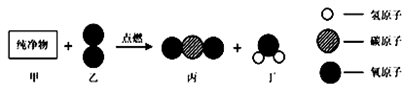
B.C:H=3:1
C.C:H:O=6:1:8
D.C:H:O=3:1:4
(1)发现和提出问题:化学反应有的很快,如爆炸,有的相当慢,如铁生锈。决定物质之间能否反应以及化学反应速率快慢的内因是反应物的结构和性质。除此以外,催化剂也能改变化学反应速率。同学们都有这样的生活经验,木炭在氧气中燃烧比在空气中燃烧的旺;这说明反应物的浓度对化学反应速率有影响。夏天,将食品放在冰箱里不容易腐烂;这说明温度对化学反应速率也有影响。那么,温度和浓度是如何影响化学反应速率?
(2)猜想与假设: a.浓度越大,化学反应的速率越快。 b.温度越高,化学反应的速率越快。
(3)收集证据:
实验仪器和试剂:试管、试管夹、酒精灯、药匙、量筒;锌粒、5%盐酸、20%盐酸。利用上述实验仪器和试剂进行探究,如果假设是a,你认为需要控制的变量有 。如果假设是b,你认为需要控制的变量有 。在实验中,通过观测 来判断反应的快慢。
(4)结论与解释:实验证明,条件相同,盐酸的溶质质量分数越大,与金属的反应速率越快。其它条件相同,温度越高,化学反应的速率越快。从反应物的微观粒子相互作用的角度,你认为其原因分别是 _______ ;__________________ 。
(5)交流与反思:通过实验探究我们知道,我们可以通过控制反应条件来控制化学反应的快慢。请你再举出一个通过控制化学反应条件来控制化学反应快慢的事例。
探究影响化学反应速率的因素。
(1)发现和提出问题:
化学反应有的很快,如爆炸,有的相当慢,如铁生锈。决定物质之间能否反应以及化学反应速率快慢的内因是反应物的结构和性质。除此以外,催化剂也能改变化学反应速率。
同学们都有这样的生活经验,木炭在氧气中燃烧比在空气中燃烧的旺;这说明反应物的浓度对化学反应速率有影响。夏天,将食品放在冰箱里不容易腐烂;这说明温度对化学反应速率也有影响。那么,温度和浓度是如何影响化学反应速率?
(2)猜想与假设:![]() .浓度越大,化学反应的速率越快。
.浓度越大,化学反应的速率越快。
![]() .温度越高,化学反应的速率越快。
.温度越高,化学反应的速率越快。
(3)收集证据:
实验仪器和试剂:试管、试管夹、酒精灯、药匙、量筒;锌粒、5%盐酸、20%盐酸。
利用上述实验仪器和试剂进行探究,如果假设是![]() ,你认为需要控制的变量有 。
,你认为需要控制的变量有 。
如果假设是![]() ,你认为需要控制的变量有 。
,你认为需要控制的变量有 。
在实验中,通过观测 来判断反应的快慢。
(4)结论与解释:实验证明,条件相同,盐酸的溶质质量分数越大,与金属的反应速率越快。其它条件相同,温度越高,化学反应的速率越快。从反应物的微观粒子相互作用的角度,你认为其原因分别是________________________________
和__________________
(5)交流与反思:通过实验探究我们知道,我们可以通过控制反应条件来控制化学反应的快慢。请你再举出一个通过控制化学反应条件来控制化学反应快慢的事例。
__________________
查看习题详情和答案>>