摘要: (2)①2Na2O2+2CO2 2Na2CO3+O2 ②2Mg+CO22MgO+C ③3MgCO3·Mg(OH)2或Mg4(OH)2(CO3)3等, 3MgCO3·Mg(OH)2+8HCl 4MgCl2+3CO2↑+4H2O
网址:http://m.1010jiajiao.com/timu3_id_62738[举报]
(1)298K、100kPa时,C(s,石墨)+O2(g)═CO2(g)△H1=-393.5kJ?mol-1 2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ?mol-1 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ?mol-1,请写出298K时由C(s,石墨)和H2(g)生成1molC2H2(g)的热化学方程式
(2)水是生命之源,也是化学反应中的主角.试回答下列问题:A.B.C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A.B.C与水反应的化学方程式:
(3)写出硫化钠在水溶液中水解的离子方程式
(4)明矾可做净水剂是因为
(5)下列哪些事实能说明醋酸是弱酸
①醋酸不易腐蚀衣服;
②0.1mol/L的CH3COONa溶液的PH约为9;
③进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多;
④0.1mol/L的CH3COOH溶液PH约为2.9;
⑤相同体积的PH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多;
⑥镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率但不改变产生气体的总量.
查看习题详情和答案>>
C(s,石墨)+H2(g)=C2H2(g)△H=226.7kJ?mol-1
C(s,石墨)+H2(g)=C2H2(g)△H=226.7kJ?mol-1
;(2)水是生命之源,也是化学反应中的主角.试回答下列问题:A.B.C是中学化学常见的三种有色物质(其组成的元素均属短周期元素),它们均能与水发生氧化还原反应,但水既不是氧化剂也不是还原剂,请写出A.B.C与水反应的化学方程式:
3NO2+H2O=2HNO3+NO、Cl2+H2O=HCl+HClO、2Na2O2+2H2O=4NaOH+O2↑
3NO2+H2O=2HNO3+NO、Cl2+H2O=HCl+HClO、2Na2O2+2H2O=4NaOH+O2↑
;(3)写出硫化钠在水溶液中水解的离子方程式
S2-+H2O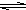 HS-+OH-
HS-+OH-
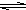 HS-+OH-
HS-+OH-S2-+H2O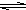 HS-+OH-
HS-+OH-
在配制硫化钠溶液时,为了防止发生水解,可以加入少量的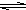 HS-+OH-
HS-+OH-NaOH
NaOH
;(4)明矾可做净水剂是因为
Al3+水解产生的胶状的Al(OH)3具有吸附性,可以吸附水中的杂质
Al3+水解产生的胶状的Al(OH)3具有吸附性,可以吸附水中的杂质
,有关的离子方程式为Al3++3H2O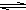 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生
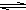 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生Al3++3H2O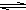 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生
;向明矾的水溶液中加入饱和的小苏打溶液,则观察到的现象是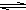 Al(OH)3+3H+有无色气体和白色絮状沉淀产生
Al(OH)3+3H+有无色气体和白色絮状沉淀产生有无色气体和白色絮状沉淀产生
有无色气体和白色絮状沉淀产生
,有关的离子方程式3HCO3-+Al3+=Al(OH)3↓+CO2↑
3HCO3-+Al3+=Al(OH)3↓+CO2↑
;(5)下列哪些事实能说明醋酸是弱酸
②④⑤⑥
②④⑤⑥
①醋酸不易腐蚀衣服;
②0.1mol/L的CH3COONa溶液的PH约为9;
③进行中和滴定时,等体积等物质的量浓度的H2SO4溶液比等体积等物质的量浓度的CH3COOH溶液消耗的NaOH溶液多;
④0.1mol/L的CH3COOH溶液PH约为2.9;
⑤相同体积的PH均等于4的盐酸和CH3COOH溶液,被同一物质的量浓度的NaOH溶液中和,CH3COOH溶液消耗的NaOH溶液多;
⑥镁粉与一定量稀硫酸反应,如果向其中加入少量醋酸钠可以降低反应速率但不改变产生气体的总量.
下列为元素周期表中的一部分,除注明外其他都用化学用语回答下列问题:
(1)8种元素中,化学性质最不活泼的是
(2)①②⑤的最高价氧化物对应水化物的碱性由强到弱的顺序为
(3)②③④中形成的简单离子半径由大到小的顺序为
(4)⑥的氢化物常温下与元素②的过氧化物反应的离子方程式为
(5)①和⑥形成的淡黄色固体的电子式为
 ,所含化学键的类型为(填“离子键”或“共价键”)
,所含化学键的类型为(填“离子键”或“共价键”)
(6)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
查看习题详情和答案>>
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
0 |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ||||
| 4 | ② | ④ |
Ar
Ar
;非金属性最强的是F
F
;(2)①②⑤的最高价氧化物对应水化物的碱性由强到弱的顺序为
KOH>NaOH>Al(OH)3
KOH>NaOH>Al(OH)3
;(3)②③④中形成的简单离子半径由大到小的顺序为
K+>Ca2+>Mg2+
K+>Ca2+>Mg2+
;(4)⑥的氢化物常温下与元素②的过氧化物反应的离子方程式为
2H2O+2Na2O2=4Na++4OH-+O2↑
2H2O+2Na2O2=4Na++4OH-+O2↑
;(5)①和⑥形成的淡黄色固体的电子式为


离子键和共价键
离子键和共价键
;(6)①和⑤的最高价氧化物对应水化物相互反应的离子方程式为
OH-+Al(OH)3 =AlO2-+2H2O
OH-+Al(OH)3 =AlO2-+2H2O
.在呼吸面具和潜水艇中可以用过氧化钠作为供氧剂.某化学探究学习小组选用适当的化学试剂和实验用品,用图中实验装置,进行实验来证明过氧化钠可作供氧剂.其中,A是实验室制取CO2的装置,D中装有过氧化钠固体.

(1)写出A装置中发生反应的离子方程式:
(2)填写表中空格:
(3)若无C装置,对实现该实验目的是否有影响
(4)试管F中收集满气体并从水中取出后,下一步实验操作为:
查看习题详情和答案>>

(1)写出A装置中发生反应的离子方程式:
CaCO3+2H+=Ca2++H2O+CO2↑
CaCO3+2H+=Ca2++H2O+CO2↑
;(2)填写表中空格:
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2中的HCl 除去CO2中的HCl |
| C | 浓硫酸 浓硫酸 |
除去CO2中的水蒸气 |
| E | NaOH溶液 NaOH溶液 |
除去O2中的CO2 除去O2中的CO2 |
否
否
(填“是”或“否”),原因2Na2O2+2H2O=4NaOH+O2
2Na2O2+2H2O=4NaOH+O2
;(4)试管F中收集满气体并从水中取出后,下一步实验操作为:
立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气
立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气
. 实验目的:探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后退色的原因.
实验目的:探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后退色的原因.【分析与猜想】
(1)根据过氧化钠与水反应的原理:2Na2O2+2H2O═4NaOH+O2↑,往过氧化钠固体完全溶解反应后的溶液中滴加酚酞本应只会变红而不会退色,而实验中发现酚酞变红后又退色.由此提出如下的猜想:
A.氧气有漂白性
B.氢氧化钠有漂白性
C.
【实验与判断】
请完成表格:
| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 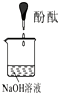 |
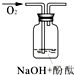 |
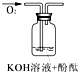 |
| 验证猜想 | C | ||
| 实验现象 | 溶液变红后不退色 | ||
| 实验说明 | 1、2的实验中NaOH溶液是用 | ||
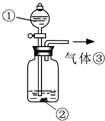
(3)可用如图装置对溶液中不很稳定的物质进行探究,在①处装入的物质是
A.酚酞试剂
B.过氧化钠与水反应后的溶液
C.二氧化锰
D.氢氧化钠固体配制的溶液
(4)气体③是