摘要:(1)相同质量时.氢气放出的热量多,产物为水.无污染 (2)H2 (3)H2O(l)+1/2O2(l) H2O(g),△H=-237.46kJ/mol 5.94×108 (4)负极:2H2+4OH--4e- 4H2O正极:O2+2H2O+4e- 4OH- 总反应式:2H2+O2 2H2O ①阴极反应为:Cu2++2e-=Cu 2H++2e-=H2↑ 当阴极收集到氢气0.112L时.铜已反应完全.共转移电子0.03mol. 此时阳极2Cl--2e-=Cl2↑反应恰好完全. 溶液中剩余的[OH-]=0.1mol/L.溶液PH=13. ②设消耗H2和O2的质量分别为x.y. 2H2 + O2 2H2O ~ 4e- 4g 32g 4mol x y 0.03mol 解得:x=0.03g y=0.24g 所以.消耗H2 0.03g,消耗O2 0.24g.
网址:http://m.1010jiajiao.com/timu3_id_59401[举报]
氢气、一氧化碳、辛烷(C8H18)、甲烷燃烧的热化学方程式分别为:
H2(g)+
O2(g)=H2O(l);△H=-285.8kJ/mol
CO(g)+
O2(g)=CO2(g);△H=-282.6kJ/mol
C8H18(l)+
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
C8H18(l)+
| 25 |
| 2 |
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
查看习题详情和答案>>
氢气、一氧化碳、辛烷(C8H18)、甲烷燃烧的热化学方程式分别为:
H2(g)+
O2(g)=H2O(l);△H=-285.8kJ/mol
CO(g)+
O2(g)=CO2(g);△H=-282.6kJ/mol
C8H18(l)+
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
查看习题详情和答案>>
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
C8H18(l)+
| 25 |
| 2 |
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
| A.H2(g) | B.CO(g) | C.C8H18(l) | D.CH4(g) |
氢气、一氧化碳、辛烷(C8H18)、甲烷燃烧的热化学方程式分别为:
H2(g)+ O2(g)=H2O(l);△H=-285.8kJ/mol
O2(g)=H2O(l);△H=-285.8kJ/mol
CO(g)+ O2(g)=CO2(g);△H=-282.6kJ/mol
O2(g)=CO2(g);△H=-282.6kJ/mol
C8H18(l)+ O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
A.H2(g)
B.CO(g)
C.C8H18(l)
D.CH4(g)
查看习题详情和答案>>
H2(g)+
 O2(g)=H2O(l);△H=-285.8kJ/mol
O2(g)=H2O(l);△H=-285.8kJ/molCO(g)+
 O2(g)=CO2(g);△H=-282.6kJ/mol
O2(g)=CO2(g);△H=-282.6kJ/molC8H18(l)+
 O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/molCH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
A.H2(g)
B.CO(g)
C.C8H18(l)
D.CH4(g)
查看习题详情和答案>>
氢气、一氧化碳、辛烷(C8H18)、甲烷燃烧的热化学方程式分别为:
H2(g)+ O2(g)=H2O(l);△H=-285.8kJ/mol
O2(g)=H2O(l);△H=-285.8kJ/mol
CO(g)+ O2(g)=CO2(g);△H=-282.6kJ/mol
O2(g)=CO2(g);△H=-282.6kJ/mol
C8H18(l)+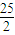 O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
A.H2(g)
B.CO(g)
C.C8H18(l)
D.CH4(g)
查看习题详情和答案>>
H2(g)+
 O2(g)=H2O(l);△H=-285.8kJ/mol
O2(g)=H2O(l);△H=-285.8kJ/molCO(g)+
 O2(g)=CO2(g);△H=-282.6kJ/mol
O2(g)=CO2(g);△H=-282.6kJ/molC8H18(l)+
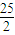 O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/mol
O2(g)=8CO2(g)+9H2O(l);△H=-5472kJ/molCH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-889.6kJ/mol
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是( )
A.H2(g)
B.CO(g)
C.C8H18(l)
D.CH4(g)
查看习题详情和答案>>
|
氢气、一氧化碳、辛烷(C8H18)、甲烷燃烧的热化学方程式分别为: H2(g)+ CO(g)+ C8H18(l)+ CH4(g)+2O2(g) 相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最多的是 | |
| [ ] | |
A. |
H2(g) |
B. |
CO(g) |
C. |
C8H18(l) |
D. |
CH4(g) |
 8CO2(g)+9H2O(l);ΔH=-5472 kJ/mol
8CO2(g)+9H2O(l);ΔH=-5472 kJ/mol CO2(g)+2H2O(l);ΔH=-889.6 kJ/mol
CO2(g)+2H2O(l);ΔH=-889.6 kJ/mol