摘要:17.图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如下图.试回答: (1)第三周期11一18号元素原子最外层电子 数变化的趋势是 . (2)图中He与Ne.Ar原子最外层电子数不一样.但都处在每周期的结尾处.从原子结构上分析其原因 . (3)原子的核外电子排布.特别是最外层的电 子数目.与元素的化学性质有密切关系.在一个化学反应中.如果有元素化合价升高.同时就有元素化合价降低. (4)探究钾元素单质与水反应的生成物.甲同学猜想生成物为KOH和 H2,乙同学猜想生成物为KOH和O2.你认为 同学的猜想不合理.请从化合价的角度解释原因 .
网址:http://m.1010jiajiao.com/timu3_id_5798[举报]
图表是整理数据.发现其中规律的一种重要工具。1一18号元素原子最外层电子数与原子序数的关系如下图。试回答:
(1)第三周期11一18号元素原子最外层电子 数变化的趋势是 。
(2)图中He与Ne.Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因 。
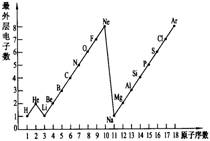
 图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
图表是整理数据.发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:(1)第三周期11一18号元素原子最外层电子 数变化的趋势是
最外层电子数依次递增
最外层电子数依次递增
.(2)图中He与Ne.Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因
都达到了相对稳定结构
都达到了相对稳定结构
.(3)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系.

图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如图.试回答:
(1)图中2和S的化学性质相似的是
(2)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钠元素的单质与水反应的生成物.甲同学猜想生成物为NaOH和H2;乙同学猜想生成物为NaOH和O2,你认为
(3)图1是1一18号元素中部分粒子的结构示意图

其中属于同种元素的是
查看习题详情和答案>>
(1)图中2和S的化学性质相似的是
O
O
.(用元素符号填空)(2)在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.探究钠元素的单质与水反应的生成物.甲同学猜想生成物为NaOH和H2;乙同学猜想生成物为NaOH和O2,你认为
乙
乙
同学的猜想不合理,请从化合价的角度解释原因若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
若生成NaOH和O2,则该反应中钠元素的化合价由0价升高到十l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
.(3)图1是1一18号元素中部分粒子的结构示意图

其中属于同种元素的是
③④
③④
(填序号); ①和④两种元素组成的化合物的化学式是Na2O
Na2O
; ⑤的原子核内的中子数比核外电子数多1个,则它的相对原子质量是31
31
.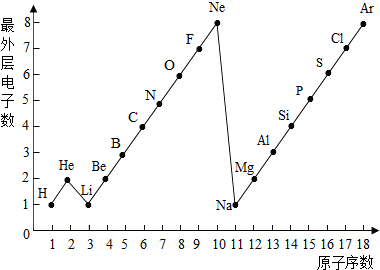 图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:
图表是整理数据、发现其中规律的一种重要工具.1一18号元素原子最外层电子数与原子序数的关系如右图.试回答:(1)图中与N元素原子最外层电子数相同的元素是
P
P
;在3一10号元素原子最外层电子数变化的趋势是由1增加到8
由1增加到8
;(2)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因
He排2个电子,最外层也达到相对稳定结构
He排2个电子,最外层也达到相对稳定结构
;(3)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系.
钠原子核内有11个质子,原子核外有
11
11
电子钠原子在化学反应中易失
失
(填“得”或“失”)电子钠元素和氯元素所组成化合物的化学式为NaCl
NaCl
(4)已知在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低.现探究钾元素(原子序数为19)单质与水反应的生成物.甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为
乙
乙
同学的猜想不合理. 图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:
图表是整理数据、发现其中规律的一种重要工具,周期表中1---18号元素最外层电子数与原子序数的关系如图所示,试回答:(1)第三周期11--18号元素原子最外层电子数变化趋势是
逐渐递增(或从1到8逐渐递增)
逐渐递增(或从1到8逐渐递增)
(2)图中He、Ne、Ar 最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因是
最外层都已达到相对稳定结构
最外层都已达到相对稳定结构
.(3)原子的最外层上的电子数目与元素的化学性质有密切关系.钠原子在化学反应中易
失
失
(填“得”或“失”)去电子,它与氯元素组成的化合物的化学式为NaCl
NaCl
(4)在一个化学反应中,如果元素的化合价升高,同时就有元素化合价降低.甲、乙两同学探究元素钠单质与水反应的生成物,甲同学猜想生成物为NаOH和H2;乙同学猜想生成物为NаOH和O2,你认为
乙
乙
猜想不合理,请从化合价变化的角度解释原因是若生成KOH和O2,则该反应中钾元素的化合价由0价升高到+l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
若生成KOH和O2,则该反应中钾元素的化合价由0价升高到+l价,氧元素的化合价由-2价升高到0价,只有元素化合价升高,没有元素化合价降低
.