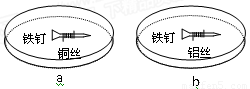
摘要:4.如右图所示.将4mol SO2和2molO2混合置于体积可变的等压容器中.在一定温度下发生如下反应:2SO2(g)+O2(g) 2SO3(g),△H<0.该反应达到平衡状态A时.测得气体总物质的量为4.2mol. 若SO2.O2.SO3的起始物质的量分别用a.b.c表示.回答下列问题: (1)在达到平衡状态A的容器中通入少量O2.体系中SO2的体积分数 .若要使SO2的体积分数再变到与平衡状态A相同.可采取的措施有: 或 . (2)若起始时a=1.2mo1.b=0.6mo1.且达到平衡后各气体的体积分数与平衡状态A相同.则起始时c的取值为 . (3)若要使反应开始时向逆反应方向进行.且达到平衡后各气体的物质的量与平衡状态A相同.则起始时c的取值范围为 . 检测提高
网址:http://m.1010jiajiao.com/timu3_id_57316[举报]
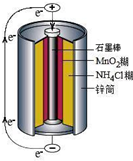 锌锰干电池是最早使用的化学电池,其基本构造如图所示.
锌锰干电池是最早使用的化学电池,其基本构造如图所示.(1)锌锰干电池的负极是
Zn
Zn
,电路中每通过0.2mole-,负极质量减少6.5
6.5
g;工作时NH4+离子在正极放电产生两种气体,其中一种气体分子是含10e-的微粒,正极的电极反应式是2NH4++2e-=2NH3↑+H2↑
2NH4++2e-=2NH3↑+H2↑
.(2)某研究小组对电池内黑色糊状物进行了下列实验.
电池内黑色糊状物粉末
无色溶液
溶解过滤
黑色残渣
已知:Zn(OH)2是两性氢氧化物.完成下列实验报告.
| 实验步骤 | 实验现象 | 实验结论和解释 | ||||||||
| 取少量上述无色溶液于试 管中,逐滴加入NaOH溶液,直至过量,再加热 | 生成白色沉淀, 白色沉淀消失, 白色沉淀消失, 产生有刺激性气味的气体 产生有刺激性气味的气体 |
无色溶液中存在Zn2+、NH4+离子 检验NH4+离子存在的离子方程式是 NH4++OH-
NH4++OH-
|
| 序号 | 烧瓶中的物质 | 实验记录 | 实验结论与解释 |
| 实验一 | 足量MnO2 | 收集到56mL气体 | MnO2做催化剂 |
| 实验二 | 足量MnO2和稀硫酸 | 黑色粉末部分溶解, 收集到112mL气体 |
MnO2做氧化剂,生成Mn2+离子 |
1:1
1:1
,实验二中反应的离子方程式为H2O2+2H++MnO2=Mn2++2H2O+O2↑
H2O2+2H++MnO2=Mn2++2H2O+O2↑
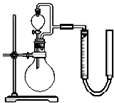
.(12分)舍勒发现氯气的的方法至今还是实验室制取氯气的主要方法之一.
(1)请写出实验室制氯气的反应化学方程 ,
(2)反应方程式中氧化剂和还原剂物质的量之比为 ;其中Cl2是 产物(填氧化或还原);
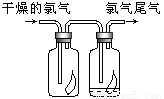
(3)如右图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是 ,从而得出的结论是 .
(4)实验室中剩余的Cl2尾气通常用NaOH溶液吸收,发生反应的离子方程式 。
查看习题详情和答案>>
如右图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C。当闭合开关S后,以下表述正确的是( )

A.电流表指针不发生偏转
B.Al、Pt两极有H2产生
C.甲池pH减小,乙池pH增加
D.Mg、C两极生成的气体在一定条件下可以恰好完全反应
查看习题详情和答案>>