摘要:A 2.BD 3.A 讲析:1.R2+离子的质子数为(A-N).氧化物的化学式为RO.摩尔质量为g/mol.所以选项A符合题意. 2.若某元素有两种核素aX.bX.则构成的双原子单质分子有 三种.若a〈b.则2a=158.2b=162.求得两种核素的质量数分别为79.81. 3.据电子层结构特征推知X为第IA族元素.Y为P.Z为O.再据化合价法则分析选项得出结论.
网址:http://m.1010jiajiao.com/timu3_id_56841[举报]
下表是元素周期表的一部分,有关说法不正确的是
|
| ⅠA | ⅡA | 部分省略 | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | d | |||||||
| 3 | a | b | c | e | f |
A.a、b、d、f四种元素的离子半径:f>d>a>b
B.元素b的单质不能与酸性氧化物发生化学反应
C.元素c的氧化物既能与酸反应又能与碱反应
D.a、c、e的最高价氧化物对应水化物之间能够相互反应
查看习题详情和答案>>A、B、C、D、E、F六种元素在周期表中的位置如图所示,下列说法正确的是( )
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
A |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
|
|
|
D |
|
|
3 |
B |
|
|
|
E |
C |
F |
|
A.热稳定性:A2C>AD
B.EF3分子中所有原子均达到8电子稳定结构,且属于非极性分子
C.六种元素中的某些元素可以形成既含共价键又含离子键的化合物
D.晶体熔点:BF<BD
查看习题详情和答案>>
A、B、C、D、E、F六种元素在周期表中的位置如图所示,下列说法正确的是( )
| 族 周期 | IA |
| 0 | |||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
| 2 |
|
|
|
|
|
| D |
|
| 3 | B |
|
|
| E | C | F |
|
A.热稳定性:A2C>AD
B.EF3分子中所有原子均达到8电子稳定结构,且属于非极性分子
C.六种元素中的某些元素可以形成既含共价键又含离子键的化合物
D.晶体熔点:BF<BD
查看习题详情和答案>>
已知下列物质的结构
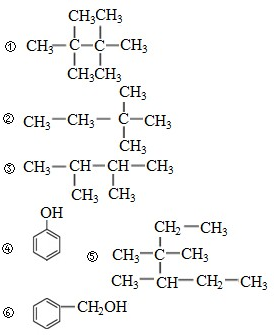
(1)其中互为同分异构体的是 (填序号).
(2)能与FeCl3溶液反应是紫色的是 (填序号).
(3)下列对⑤的命名正确的是 (填序号).
A.2,3-二甲基-2-乙基戊烷
B.3,4,4-三甲基乙烷
C.3,3,4-三甲基己烷
D.2,3-二甲基-3-乙基戊烷. 查看习题详情和答案>>

(1)其中互为同分异构体的是
(2)能与FeCl3溶液反应是紫色的是
(3)下列对⑤的命名正确的是
A.2,3-二甲基-2-乙基戊烷
B.3,4,4-三甲基乙烷
C.3,3,4-三甲基己烷
D.2,3-二甲基-3-乙基戊烷. 查看习题详情和答案>>
T1℃时,向容积为2L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
(1)用H2表示反应在t1min内的平均速率为v(H2)=
mol/(L?min)
mol/(L?min).
(2)保持其他条件不变,若起始时向容器中充入1.50molCO和1.00molH2O(g),达到平衡时,n(CO2)=
(3)保持其他条件不变,在t2时向容器中再通入0.50molCO,与原平衡相比,达到新平衡时CO转化率将
(4)保持其他条件不变,若起始时向容器中充入amolCO和bmolH2O(g),达到平衡时,CO2的体积分数为24%,a、b的值须满足的条件是
(5)温度升至T2℃,上述反应的平衡常数为0.64,则正反应的△H
查看习题详情和答案>>
| 反应时间 | H2O | CO |
| 0 | 1.00 | 1.50 |
| t1 | 0.40 | |
| t2 | 0.90 |
| 0.3 |
| t1 |
| 0.3 |
| t1 |
(2)保持其他条件不变,若起始时向容器中充入1.50molCO和1.00molH2O(g),达到平衡时,n(CO2)=
0.60 mol
0.60 mol
.(3)保持其他条件不变,在t2时向容器中再通入0.50molCO,与原平衡相比,达到新平衡时CO转化率将
减小
减小
(填增大或减小,下同),H2O的体积分数将减小
减小
.(4)保持其他条件不变,若起始时向容器中充入amolCO和bmolH2O(g),达到平衡时,CO2的体积分数为24%,a、b的值须满足的条件是
a:b=3:2或 b:a=2:3
a:b=3:2或 b:a=2:3
.(5)温度升至T2℃,上述反应的平衡常数为0.64,则正反应的△H
<
<
0(填>或<).