摘要:A 解析: A中.HCOOC2H5+H2OHCOOH+C2H5OH 生成的HCOOH和C2H5OH相对分子质量都是46 , B项.水解产物相对分子质量不同. 葡萄糖不水解.而淀粉水解只生成一种物质不符合题意.
网址:http://m.1010jiajiao.com/timu3_id_55539[举报]
将氯气通入含有下列大量离子的各组溶液中,无明显现象的是( B )
A. H+、Ag+、NO![]() B. Na+、OH-、Cl-
B. Na+、OH-、Cl-
C. K+、HCO![]() 、NO
、NO![]() D. K+、SO
D. K+、SO![]() 、Bl-
、Bl-
【解析】 A会生成氯化银的沉淀;C会产生二氧化碳气体;D会生成溴单质而出现颜色;B虽然会与氯气反应,但无明显现象。故选B。
查看习题详情和答案>>某溶液中含有HCO
、CO
、SO
、Na+、NO
五种离子.若向其中加入Na2O2粉末充分反应后(溶液体积变化忽略不计),溶液中离子浓度保持不变的是( )
- 3 |
2- 3 |
2- 3 |
- 3 |
 最近雾霾天气肆虐我国大部分地区.其中SO2是造成空气的污染的主要原因,利用钠碱循环法可除去SO2.
最近雾霾天气肆虐我国大部分地区.其中SO2是造成空气的污染的主要原因,利用钠碱循环法可除去SO2.(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7;H2CO3的电离常数为K1=4.30×10-7,K2=5.60×10-11,则下列微粒可以大量共存的是
A.C
| O | 2- 3 |
| O | - 3 |
| O | - 3 |
| O | 2- 3 |
N(SO
|
91:9 | 1:1 | 1:91 | ||||
| pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显
②在NaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)═2c(SO
2- 3 |
- 3 |
B.c(Na+)>c(HSO
- 3 |
2- 3 |
C.c(H2SO3)+c(H+)═c(SO
2- 3 |
D.c(Na+)+c(H+)═2c(SO
2- 3 |
- 3 |
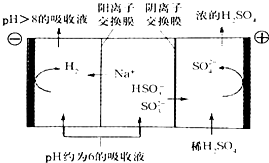
(4)当吸收液的pH降至约为6时,需送至电解槽处理,直至得到pH>8的吸收液再循环利用,电解示意图如图所示:
①写出阳极上发生的电极反应式
②当电极上有1mol电子转移时阴极产物的质量为
(2013?金华模拟)有A、B、C、D四种强电解质,它们在水中电离产生的离子如下表(每种物质只含一种阴离子且互不重复).
①A、C溶液的pH均大于7,A、B溶液中水的电离程度比纯水大; ②C溶液和D溶液混合时只产生白色沉淀,B溶液和C溶液混合时只产生刺激性气味的气体,A溶液和D溶液混合时无明显现象. 有关说法不正确的是( ) |
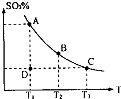 (1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:
(1)在硫酸生产中,SO2催化氧化生成SO3是反应的关键,其反应的化学方程式为:2SO2(g)+O2(g)?2SO2(g),反应混合体系SO3的百分含量和温度的关系如图所示(曲线上任何一点都表示平衡状态),根据图示回答下列问题:①反应2SO2(g)+O2(g)?2SO2(g)的△H
②若温度为T1、T2,反应的平衡常数分别为K1K2 则K1
③在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10mol O2,在500℃开始反应,半分钟达到平衡,测得容器内含SO3 0.18mol,则v(O2)=
(2)已知三种无色溶液:a.NaHCO3溶液,b.AlCl3溶液,c.NaAlO2溶液,它们两两反应均能生成Al(OH)3沉淀.请回答下列问题:
①两种溶液恰好完全反应,所得溶液中c(OH-)=
| Kw |
②能体现出NaHCO3在反应中,HCO-3的水解程度小于电离程度的离于方程式为