摘要:28.Fe2O3 +2AlAl 2O3 + 2 Fe (2)①③④ (3)N2O3+ 2OH- + 2H2O2 = 2NO3- + 3H2O (4)150或350 ②cdba
网址:http://m.1010jiajiao.com/timu3_id_55202[举报]
某混和物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质之间的变化:
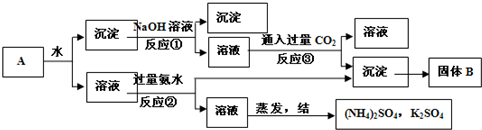
据此判断:
(1)固体B的所含物质的化学式 ;
(2)反应①的离子方程式 ;
(3)反应②的离子方程式 ;
(4)反应③的离子方程式 .
查看习题详情和答案>>

据此判断:
(1)固体B的所含物质的化学式
(2)反应①的离子方程式
(3)反应②的离子方程式
(4)反应③的离子方程式
工业从铝土矿(主要成分是Al2O3?xH2O、SiO2、Fe2O3等)提取纯Al2O3做冶炼铝的原料,提取时操作过程如图,图中操作错误的是( )
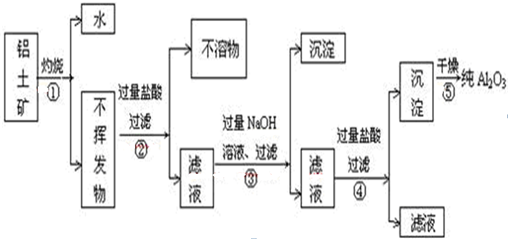

| A、④⑤ | B、③④ | C、②⑤ | D、①② |
工业常用高温分解FeSO4的方法制备Fe2O3,其化学方程式为:
2FeSO4
Fe2O3+SO2↑+SO3↑
为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解后的固体加入稀盐酸溶解,为了检验溶液中是否有Fe3+,还需要向溶液中加入 溶液,如有 现象则证明有Fe3+.
(2)将分解产生的气体通入下图所示的装置中:
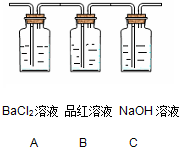
请回答下列问题:
如在装置 中,发现有 现象,则证明有SO3;
如在装置 中,发现有 现象则证明有SO2.
(3)装置中的NaOH溶液的作用是 .
请写出相应反应的离子方程式 .
查看习题详情和答案>>
2FeSO4
| ||
为检验FeSO4高温分解的产物,进行如下实验:
(1)取少量分解后的固体加入稀盐酸溶解,为了检验溶液中是否有Fe3+,还需要向溶液中加入
(2)将分解产生的气体通入下图所示的装置中:

请回答下列问题:
如在装置
如在装置
(3)装置中的NaOH溶液的作用是
请写出相应反应的离子方程式
铝是一种重要的金属,在生产、生活中具有许多重要的用途,如图是从铝土矿中制备铝的工艺流程:
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质.
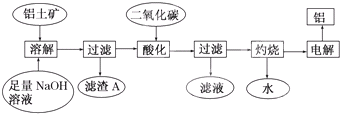
回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式 ,滤渣A的主要成分为 .
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是 ,通入过量的二氧化碳时,生成沉淀的离子方程式为 .
(3)电解氧化铝,每生成1molAl时,生成 g氧气.
查看习题详情和答案>>
已知:铝土矿的主要成分是Al2O3,此外还含有少量Fe2O3等杂质.

回答下列问题:
(1)写出向铝土矿中加入足量氢氧化钠溶液后,该步操作中铝土矿主要成分发生反应的离子方程式
(2)在工艺流程第三步中,选用二氧化碳作酸化剂而不使用盐酸的原因是
(3)电解氧化铝,每生成1molAl时,生成
 [化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.
[化学--选修物质结构与性质]不锈钢以其优异的抗腐蚀性能越来越受到人们的青睐,它主要是由铁、铬、镍、铜、碳等元素所组成的合金.(1)写出Fe2+的核外电子排布式
(2)[cr(H2O)4Cl2]Cl?2H2O中cr的配位数为
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)n,推测Ni(CO)n的晶体类型
(4)常温下,碳与氢以原子个数比1:1形成的气态氢化物中,其分子中的σ键和П键的数目比是
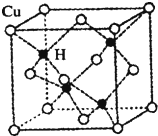
(5)铜是第四周期最重要的过渡元素之一,其单质及化合物具有广泛用途.CuH的晶体结构如右图所示,若CuH的密度为d g/cm3,阿伏加德罗常数的值为NA,则该晶胞的边长为