摘要:某校科技活动小组用镁粉.盐酸.醋酸及设计的右图装置.对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究. (1)组装完成后.某同学发现该装置在设计上存在明显缺陷:根本无法完成实验.甚至存在危险.其缺陷在于 .其改进方法是 . (2)改进装置后.检查一侧装置的气密性的方法是 . (3)欲配制100mL实验所需浓度的盐酸.除50mL量筒.烧杯.酸式滴定管.胶头滴管之外.还需用到的主要玻璃仪器是 . 正确操作.记录得到下表中部分实验数据.分析数据.观察实验装置图.回答下列问题: A烧瓶中 B烧瓶中 20℃.101kPa 50mL量筒内气体读数 反应时间 A瓶 B瓶 40mL0.1mol/L 醋酸溶液 40mL0.1mol/L 盐酸溶液 5mL t(a1)=155s t(b1)=7s 10mL t(a2)=310s t(b2)=16s 15mL t(a3)=465s t(b3)=30s 20mL t(a4)=565s t(b4)=64s -- -- -- 44.8mL t(an)=865s t(bn)=464s (4)在实验数据中:①t(a1)远远大于t(b1)的原因为: , ②由 [用含t(b1).t(b2).t(b3)代数式表示] 说明盐酸是可能不存在电离平衡,由 [用含t(a1).t(a2).t(a3)代数式表示] 说明醋酸中存在电离平衡. (5)通过该实验可得到的结论是:① ,② . 21为了探究硫化钠晶体(Na2S•nH2O)在空气中的变化.某兴趣小组的实验步骤及现象记录如下:①将少量硫化钠晶体置于表面皿上.暴露在空气中,②三天后将样品放入盛水的烧杯中.搅拌后得无色澄清溶液,③取少量该溶液加入过量盐酸中.有气体放出.且溶液保持澄清. (1)请你根据上述记录.对放出气体进行猜想: 猜想①:可能是H2S , 猜想②:可能是SO2 , 猜想③可能是CO2, 猜想④:可能是 , 猜想⑤:可能是 . (2)若放出的气体是两种气体的混合气.现有:浓.稀2种品红溶液.浓.稀2种溴水.澄清石灰水.浓.稀2种盐酸溶液.试管气体发生装置.洗气瓶.试管洗气装置.请设计一个组合实验分析混合气的组成.在下表中简要写出实验方法.现象和结论: 实验方案 可能的现象和相应的结论 (3)如果要检验硫化钠晶体是否被氧化生成了硫酸钠.请简要说明检验的方法.现象和结论: .
网址:http://m.1010jiajiao.com/timu3_id_55111[举报]
某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
(4)在实验数据中:①t(a1)远远大于t(b1)的原因为:______;
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.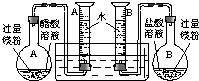
查看习题详情和答案>>
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 |
反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 |
40mL0.1mol/L 盐酸溶液 |
5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.

某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
(4)在实验数据中:①t(a1)远远大于t(b1)的原因为:______;
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于______,其改进方法是______.
(2)改进装置后,检查一侧装置的气密性的方法是______.
(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是______.
正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 | 反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 | 40mL0.1mol/L 盐酸溶液 | 5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
②由______[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由______[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.
(5)通过该实验可得到的结论是(回答出两点即可):①______;②______.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2009?肇庆二模)某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.
(2009?肇庆二模)某校科技活动小组用镁粉、盐酸、醋酸及设计的右图装置(夹持固定装置已略去),对两种酸分别与镁反应的速率以及是否存在电离平衡进行探究.(1)组装完成后,某同学发现该装置在设计上存在明显缺陷:根本无法完成实验,甚至存在危险,其缺陷在于
A、B两个量筒口用胶塞密封,反应产生的H2会造成压强过大而发生危险[或密封的量筒内气压随反应开始后不断增大,会造成烧瓶或量筒因压强过大将胶塞推出]
A、B两个量筒口用胶塞密封,反应产生的H2会造成压强过大而发生危险[或密封的量筒内气压随反应开始后不断增大,会造成烧瓶或量筒因压强过大将胶塞推出]
,其改进方法是除去A、B量筒口的胶塞
除去A、B量筒口的胶塞
.(2)改进装置后,检查一侧装置的气密性的方法是
将导管口放入水槽中,用手捂住烧瓶,如果导管口有气泡产生,松开手后导管内有一段水柱,证明装置不漏气
将导管口放入水槽中,用手捂住烧瓶,如果导管口有气泡产生,松开手后导管内有一段水柱,证明装置不漏气
.(3)欲配制100mL实验所需浓度的盐酸,除50mL量筒、烧杯、酸式滴定管、胶头滴管之外,还需用到的主要玻璃仪器是
100mL容量瓶、玻璃棒
100mL容量瓶、玻璃棒
.正确操作,记录得到下表中部分实验数据.分析数据,观察实验装置图,回答下列问题:
| A烧瓶中 | B烧瓶中 | 20℃、101kPa 50mL量筒内气体读数 |
反应时间 | |
| A瓶 | B瓶 | |||
| 40mL0.1mol/L 醋酸溶液 |
40mL0.1mol/L 盐酸溶液 |
5mL | t(a1)=155s | t(b1)=7s |
| 10mL | t(a2)=310s | t(b2)=16s | ||
| 15mL | t(a3)=465s | t(b3)=30s | ||
| 20mL | t(a4)=565s | t(b4)=64s | ||
| … | … | … | ||
| 44.8mL | t(an)=865s | t(bn)=464s | ||
开始阶段醋酸溶液中的[H+]远小于相同浓度的盐酸中的[H+]
开始阶段醋酸溶液中的[H+]远小于相同浓度的盐酸中的[H+]
;②由
t(b3)-t(b2)>t(b2)-t(b1)或t(b3)>t(b1)+t(b2)
t(b3)-t(b2)>t(b2)-t(b1)或t(b3)>t(b1)+t(b2)
[用含t(b1)、t(b2)、t(b3)代数式表示]说明盐酸是可能不存在电离平衡;由t(a3)-t(a2)=t(a2)-t(a1)或t(a3)=t(a1)+t(a2)
t(a3)-t(a2)=t(a2)-t(a1)或t(a3)=t(a1)+t(a2)
[用含t(a1)、t(a2)、t(a3)代数式表示]说明醋酸中存在电离平衡.(5)通过该实验可得到的结论是(回答出两点即可):①
相同物质的量浓度的盐酸、醋酸与金属反应时,盐酸开始反应速率大,过一段时间后醋酸较盐酸反应速率的快
相同物质的量浓度的盐酸、醋酸与金属反应时,盐酸开始反应速率大,过一段时间后醋酸较盐酸反应速率的快
;②盐酸是强电解质,醋酸是弱电解质(存在电离平衡)
盐酸是强电解质,醋酸是弱电解质(存在电离平衡)
.