网址:http://m.1010jiajiao.com/timu3_id_53829[举报]
微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能。以葡萄糖溶液作底物为例,其工作原理如图所示。
已知石墨电极上的反应为
C6H12O6+ 6H2O - 24e- ="====" 6CO2+ 24H+
(1)电池中的质子交换膜只允许质子和水分子通过。电池工作时,质子移向电池的_ __极(填正或负),铂碳上所发生的电极反应式为:___________ _ _______
(2)葡萄糖的燃烧热为2800 kJ·mol-1 ,写出葡萄糖完全燃烧的热化学方程式:_____________________________________________________________________
(3)化学需氧量(COD)是重要的水质指标.其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1 L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6 kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是__________________(填序号)
| 序号 | A | B | C | D | E |
| 污水类型 | 生活污水 | 印染 | 电镀 | 造纸 | 硫酸工业废水 |
| COD值/mg·L-1 | 520 | 870 | 20 | 960 | 120 |
微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体.将有机物的化学能转化为电能。以葡萄糖溶液作底物为例,其工作原理如图所示。

已知石墨电极上的反应为
C6H12O6+ 6H2O - 24e- ="====" 6CO2+ 24H+
(1)电池中的质子交换膜只允许质子和水分子通过。电池工作时,质子移向电池的_ __极(填正或负),铂碳上所发生的电极反应式为:___________ _ _______
(2)葡萄糖的燃烧热为2800 kJ·mol-1 ,写出葡萄糖完全燃烧的热化学方程式:_____________________________________________________________________
(3)化学需氧量(COD)是重要的水质指标.其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1 L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6 kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是__________________(填序号)
序号 A B C D E
污水类型 生活污水 印染 电镀 造纸 硫酸工业废水
COD值/mg·L-1 520 870 20 960 120
查看习题详情和答案>>

已知石墨电极上的反应为
C6H12O6+ 6H2O - 24e- ="====" 6CO2+ 24H+
(1)电池中的质子交换膜只允许质子和水分子通过。电池工作时,质子移向电池的_ __极(填正或负),铂碳上所发生的电极反应式为:___________ _ _______
(2)葡萄糖的燃烧热为2800 kJ·mol-1 ,写出葡萄糖完全燃烧的热化学方程式:_____________________________________________________________________
(3)化学需氧量(COD)是重要的水质指标.其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1 L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6 kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是__________________(填序号)
| 序号 | A | B | C | D | E |
| 污水类型 | 生活污水 | 印染 | 电镀 | 造纸 | 硫酸工业废水 |
| COD值/mg·L-1 | 520 | 870 | 20 | 960 | 120 |
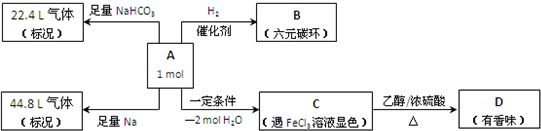
(1)已知有机物A的相对分子质量不超过180,若将A完全燃烧,只生成CO2和H2O,且n(CO2):n(H2O)=7:5,反应中消耗的O2和生成的CO2的物质的量相等,有机物A的分子式为______.
(2)根据有机物A能与NaHCO3反应放出气体,可知A分子中含有的官能团的名称是______.
(3)有机物A分子中有四个相邻的取代基,且碳碳双键上接羟基时,或者一个碳原子上同时连接2个或2个以上羟基时不能稳定存在,又知C分子的碳环上的一氯取代物只有两种结构.则B的结构简式为______.
(4)写出下列反应的化学方程式.
①A+NaHCO3(足量):______.
②CD:______.
(5)C的同分异构体中,含有三个取代基的异构体共有______种,请写出其中一种的结构简式______.
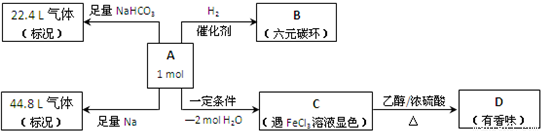
(1)已知有机物A的相对分子质量不超过180,若将A完全燃烧,只生成CO2和H2O,且n(CO2):n(H2O)=7:5,反应中消耗的O2和生成的CO2的物质的量相等,有机物A的分子式为 .
(2)根据有机物A能与NaHCO3反应放出气体,可知A分子中含有的官能团的名称是 .
(3)有机物A分子中有四个相邻的取代基,且碳碳双键上接羟基时,或者一个碳原子上同时连接2个或2个以上羟基时不能稳定存在,又知C分子的碳环上的一氯取代物只有两种结构.则B的结构简式为 .
(4)写出下列反应的化学方程式.
①A+NaHCO3(足量): .
②CD: .
(5)C的同分异构体中,含有三个取代基的异构体共有 种,请写出其中一种的结构简式 . 查看习题详情和答案>>