摘要:9. (2) (3)保护醛基不被还原. (4)RCHO + 2Ag(NH3)2+ + 2OH- RCOO- +NH4+ +2Ag↓+3NH3 + H2O (5)
网址:http://m.1010jiajiao.com/timu3_id_52103[举报]
(2011?常州三模)药物E具有抗癌抑菌功效,其合成路线如下:(B、D分子中未参加反应的部分省略)
(1)很多药物分子有手性碳而具有旋光性,A分子中有
(2)C的结构简式为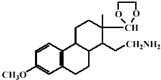
 ,E的结构简式为
,E的结构简式为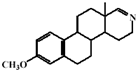
 .
.
(3)设计反应①的目的是
(4)A与银氨溶液反应的化学方程式为(A以R-CHO表示)
(5)阅读以下信息,依据以上流程图和所给信息,以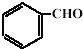 和
和 为
为
原料设计合成氨基酸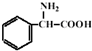 的路线.已知:
的路线.已知: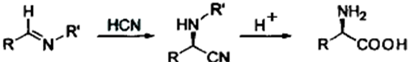
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A
B
C…→H.
 .
.
查看习题详情和答案>>

(1)很多药物分子有手性碳而具有旋光性,A分子中有
4
4
个手性碳原子.(2)C的结构简式为




(3)设计反应①的目的是
保护醛基不被还原
保护醛基不被还原
.(4)A与银氨溶液反应的化学方程式为(A以R-CHO表示)
RCHO+2Ag(NH3)2++2OH-
RCOO-+NH4++2Ag↓+3NH3+H2O
| △ |
RCHO+2Ag(NH3)2++2OH-
RCOO-+NH4++2Ag↓+3NH3+H2O
.| △ |
(5)阅读以下信息,依据以上流程图和所给信息,以
 和
和 为
为原料设计合成氨基酸
 的路线.已知:
的路线.已知:
提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A
| 反应物 |
| 反应条件 |
| 反应物 |
| 反应条件 |


对乙酰氨基酚,俗称扑热息痛(Paracetamol),具有很强的解热镇痛作用,工业上通过下列方法合成(B1和B2、C1和C2分别互为同分异构体,无机产物略去):

请按要求填空:
(1)扑热息痛中含有的官能团有
(2)写出反应①的方程式 +CH3I
+CH3I
 +HI
+HI +CH3I
+CH3I
 +HI反应类型
+HI反应类型
(3)反应②中生成的主要产物为
(4)工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是
(5)扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(Ⅰ)是对位二取代苯;(Ⅱ)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(Ⅲ)两个氧原子与同一原子相连.其中2种的结构简式是 和
和 ,写出另3种同分异构体的结构简式
,写出另3种同分异构体的结构简式
 .
.
查看习题详情和答案>>

请按要求填空:
(1)扑热息痛中含有的官能团有
肽键和酚羟基
肽键和酚羟基
(填名称),其分子中有5
5
种化学环境不同的氢原子.(2)写出反应①的方程式
 +CH3I
+CH3I| 一定条件 |
 +HI
+HI +CH3I
+CH3I| 一定条件 |
 +HI
+HI取代反应
取代反应
(3)反应②中生成的主要产物为
B1
B1
(填B1或B2),其判断的依据为基团间相互影响,分子中醚基的空间位阻大,使得对位更容易取代
基团间相互影响,分子中醚基的空间位阻大,使得对位更容易取代
(4)工业上设计反应①、②、③,而不是只通过反应②得到C1、C2,其目的是
保护酚羟基不被硝酸氧化
保护酚羟基不被硝酸氧化
.(5)扑热息痛有很多同分异构体,符合下列要求的同分异构体有5种:(Ⅰ)是对位二取代苯;(Ⅱ)苯环上两个取代基一个含氮不含碳、另一个含碳不含氮;(Ⅲ)两个氧原子与同一原子相连.其中2种的结构简式是
 和
和 ,写出另3种同分异构体的结构简式
,写出另3种同分异构体的结构简式

化合物A是石油化工的一种重要原料,用A和水煤气为原料经下列途径合成化合物D(分子式为C3H6O3).

已知:

请回答下列问题:
(1)写出下列物质的结构简式:
A:
(2)指出反应②的反应类型
(3)写出反应③的化学方程式
(4)反应④的目的是
(5)化合物D’是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物.D’在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4).请分别写出D’生成E和F的化学方程式:
D’→E:
D’→F:
 .
.
查看习题详情和答案>>

已知:

请回答下列问题:
(1)写出下列物质的结构简式:
A:
CH2=CH2
CH2=CH2
;B:CH3CH2CHO
CH3CH2CHO
;C:CH2=CHCHO
CH2=CHCHO
;D:CH2(OH)CH(OH)CHO
CH2(OH)CH(OH)CHO
.(2)指出反应②的反应类型
取代反应
取代反应
.(3)写出反应③的化学方程式
CH3CHBrCHO+NaOH
CH2=CHCHO+NaBr+H2O
| 醇 |
| △ |
CH3CHBrCHO+NaOH
CH2=CHCHO+NaBr+H2O
.| 醇 |
| △ |
(4)反应④的目的是
保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化
保护醛基,防止反应⑤时被高锰酸钾碱性溶液氧化
.(5)化合物D’是D的一种同分异构体,它最早发现于酸牛奶中,是人体内糖类代谢的中间产物.D’在浓硫酸存在的条件下加热,既可以生成能使溴水褪色的化合物E(C3H4O2),又可以生成六原子环状化合物F(C6H8O4).请分别写出D’生成E和F的化学方程式:
D’→E:
CH3CH(OH)COOH
CH2=CHCOOH+H2O
| 浓硫酸 |
| △ |
CH3CH(OH)COOH
CH2=CHCOOH+H2O
.| 浓硫酸 |
| △ |
D’→F:


(2008?广东)醇氧化成醛的反应是药物、香料合成中的重要反应之一.
(1)苯甲醇可由C6H5CH2Cl在NaOH水溶液中发生取代反应而得,反应方程式为
 .
.
(2)醇在催化剂作用下氧化成醛的反应是绿色化学的研究内容之一.某科研小组研究了把催化剂在氧气气氛中对一系列醇氧化成醛反应的催化效果,反应条件为:K2CO3、363K、甲苯(溶剂).实验结果如下:
分析表中数据,得到把催化剂催化效果的主要结论是
(3)用空气代替氧气气氛进行苯甲醇氧化生成苯甲醛的反应,其他条件相同,产率达到95%时的反应时间为7.0小时.请写出用空气代替氧气气氛进行反应的优缺点:
(4)苯甲醛易被氧化.写出苯甲醛被银氨溶液氧化的反应方程式
(5)在药物、香料合成中常利用醛和醇反应生成缩醛来保护醛基,此类反应在酸催化下进行.例如:
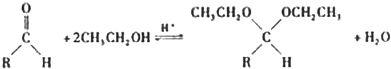
①在以上醛基保护反应中要保证反应的顺利进行,可采取的措施有
②已知具有五元环和六元环结构的缩醛比较稳定.写出用乙二醇(HOCH2CH3OH)保护苯甲醛中醛基的反应方程式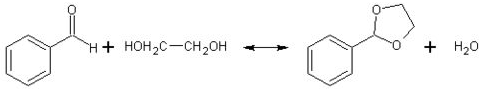
 .
.
查看习题详情和答案>>
(1)苯甲醇可由C6H5CH2Cl在NaOH水溶液中发生取代反应而得,反应方程式为


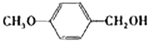
(2)醇在催化剂作用下氧化成醛的反应是绿色化学的研究内容之一.某科研小组研究了把催化剂在氧气气氛中对一系列醇氧化成醛反应的催化效果,反应条件为:K2CO3、363K、甲苯(溶剂).实验结果如下:
| 醇 | 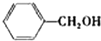 |
 |
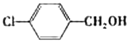 |
| 反应时间/h | 2.5 | 2.5 | 2.5 |
| 醛的产率/% | 95 | 96 | 94 |
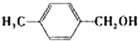
| 醇 | 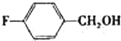 |
 |
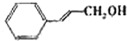 |
| 反应时间/h | 3.0 | 3.0 | 15.0 |
| 醛的产率/% | 95 | 92 | 40 |
苯环上的取代基对醛的产率影响不大,对反应时间有一定影响及与羟基相连的碳链长,大大降低醛的产率与增大反应时间
苯环上的取代基对醛的产率影响不大,对反应时间有一定影响及与羟基相连的碳链长,大大降低醛的产率与增大反应时间
(写出2条).(3)用空气代替氧气气氛进行苯甲醇氧化生成苯甲醛的反应,其他条件相同,产率达到95%时的反应时间为7.0小时.请写出用空气代替氧气气氛进行反应的优缺点:
优点为原料易得,降低成本,防止苯甲醛氧化为苯甲酸;缺点为令反应时间增长
优点为原料易得,降低成本,防止苯甲醛氧化为苯甲酸;缺点为令反应时间增长
.(4)苯甲醛易被氧化.写出苯甲醛被银氨溶液氧化的反应方程式
C6H5CHO+2Ag(NH3)2OH
C6H5COONH4+2Ag↓+3NH3↑+H2O
| 水浴加热 |
C6H5CHO+2Ag(NH3)2OH
C6H5COONH4+2Ag↓+3NH3↑+H2O
(标出具体反应条件).| 水浴加热 |
(5)在药物、香料合成中常利用醛和醇反应生成缩醛来保护醛基,此类反应在酸催化下进行.例如:
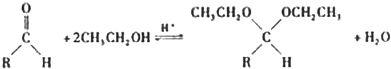
①在以上醛基保护反应中要保证反应的顺利进行,可采取的措施有
CH3CH2OH过量,令化学平衡向正反应方向移动或边反应边蒸馏缩醛脱离反应体系,令化学平衡向正反应方向移动
CH3CH2OH过量,令化学平衡向正反应方向移动或边反应边蒸馏缩醛脱离反应体系,令化学平衡向正反应方向移动
(写出2条).②已知具有五元环和六元环结构的缩醛比较稳定.写出用乙二醇(HOCH2CH3OH)保护苯甲醛中醛基的反应方程式


(2013?揭阳一模)酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式.SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如图:
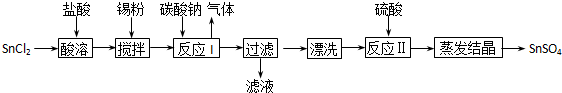
回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是
(2)反应I生成的沉淀为SnO,写出该反应的化学方程式:
(3)检验沉淀已经“洗涤”干净的操作是:
(4)反应Ⅱ硫酸的作用之一是控制溶液的pH.若溶液中c(Sn2+)=1.0mol?L-1,则室温下应控制溶液pH
(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:
(6)潮湿环境中,镀锡铜即使锡层破损也能防止形成铜绿,请结合有关的原理解释其原因:
查看习题详情和答案>>

回答下列问题:
(1)SnCl2用盐酸而不用水直接溶解的原因是
抑制Sn2+水解
抑制Sn2+水解
,加入锡粉的作用是防止Sn2+被氧化
防止Sn2+被氧化
.(2)反应I生成的沉淀为SnO,写出该反应的化学方程式:
SnCl2+Na2CO3=SnO+CO2↑+2NaCl
SnCl2+Na2CO3=SnO+CO2↑+2NaCl
.(3)检验沉淀已经“洗涤”干净的操作是:
取少量最后一次洗涤液于试管中,滴入几滴AgNO3溶液,若无白色沉淀生成,则说明沉淀已洗涤干净
取少量最后一次洗涤液于试管中,滴入几滴AgNO3溶液,若无白色沉淀生成,则说明沉淀已洗涤干净
.(4)反应Ⅱ硫酸的作用之一是控制溶液的pH.若溶液中c(Sn2+)=1.0mol?L-1,则室温下应控制溶液pH
小于1
小于1
.(已知:Ksp[Sn(OH)2]=1.0×10-26)(5)酸性条件下,SnSO4还可用作双氧水的去除剂,试写出所发生反应的离子方程式:
Sn2++H2O2+2H+=Sn4++2H2O
Sn2++H2O2+2H+=Sn4++2H2O
.(6)潮湿环境中,镀锡铜即使锡层破损也能防止形成铜绿,请结合有关的原理解释其原因:
潮湿环境中,Sn与Cu构成原电池,Sn作为负极,保护正极Cu不被氧化
潮湿环境中,Sn与Cu构成原电池,Sn作为负极,保护正极Cu不被氧化
.