摘要:1·组成:也称碳水化合物如何理解?是不是碳与水组成化合物? 2·通式:Cn(HO)m 糖类 符合通式的不一定是糖类 如:. 不符合通式的可能是糖类 如: 3·分类:按照水解的发生情况及结构特点分为:单糖.低聚糖和多糖
网址:http://m.1010jiajiao.com/timu3_id_51507[举报]
铜及其化合物在生产和生活实际中应用广泛.
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.
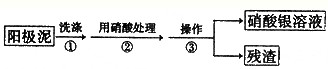
(1)操作③所需的仪器有:烧杯、
(2)为了回收金,他们查阅了有关资料如表:
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为1:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因:
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.
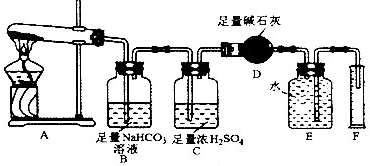
[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用
(4)根据装置E、F中现象,推测还有气体
(5)装置A中反应的化学方程式为
[实验结论]无水硫酸铜受热分解不仅仅生成Cu和SO3.
[反思与评价]
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素
查看习题详情和答案>>
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.

(1)操作③所需的仪器有:烧杯、
漏斗、玻璃棒
漏斗、玻璃棒
.(2)为了回收金,他们查阅了有关资料如表:
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3 Au(NO3)3+3NO2↑+3H2O Au(NO3)3+3NO2↑+3H2O |
<10-5 |
| 反应2 | Au3++Cl-  [AuCl4]- [AuCl4]- |
>105 |
浓盐酸含有大量氯离子,Au3+离子与氯离子形成稳定的AuCl4-离子,使反应②平衡向右移动,则金溶于王水中
浓盐酸含有大量氯离子,Au3+离子与氯离子形成稳定的AuCl4-离子,使反应②平衡向右移动,则金溶于王水中
.Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.

[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用
用来干燥气体
用来干燥气体
.(4)根据装置E、F中现象,推测还有气体
O2
O2
(填分子式)生成;实验生成的SO3为0.005
0.005
mol.(5)装置A中反应的化学方程式为
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
| ||
3CuSO4
3CuO+2SO2↑+SO3↑+O2↑
.
| ||
[实验结论]无水硫酸铜受热分解不仅仅生成Cu和SO3.
[反思与评价]
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素
装置内部有气体滞留,气体吸收不完全;称量造成的误差
装置内部有气体滞留,气体吸收不完全;称量造成的误差
(任写2点)铜及其化合物在生产和生活实际中应用广泛.
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.
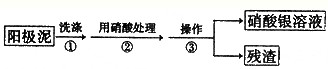
(1)操作③所需的仪器有:烧杯、______.
(2)为了回收金,他们查阅了有关资料如表:
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3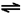 Au(NO3)3+3NO2↑+3H2O Au(NO3)3+3NO2↑+3H2O | <10-5 |
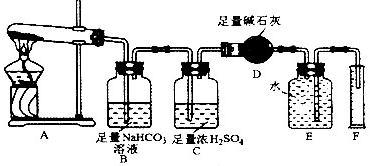
| 反应2 | Au3++Cl- 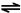 [AuCl4]- [AuCl4]- | >105 |
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.
[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用______.
(4)根据装置E、F中现象,推测还有气体______(填分子式)生成;实验生成的SO3为______ mol.
(5)装置A中反应的化学方程式为______.
[实验结论]无水硫酸铜受热分解不仅仅生成Cu和SO3.
[反思与评价]
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素______(任写2点) 查看习题详情和答案>>
铜及其化合物在生产和生活实际中应用广泛.
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.
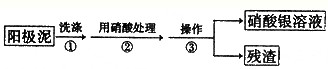
(1)操作③所需的仪器有:烧杯、______.
(2)为了回收金,他们查阅了有关资料如表:
从资料中可知,常温下金很难与硝酸反应,但却可溶于王水(浓硝酸与浓盐酸体积比为1:3的混合物).请你运用化学平衡移动原理,简要说明金能溶于王水的原因:______.
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.
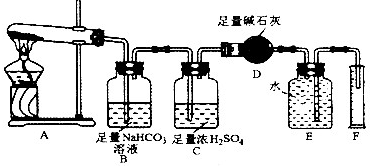
[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用______.
(4)根据装置E、F中现象,推测还有气体______(填分子式)生成;实验生成的SO3为______ mol.
(5)装置A中反应的化学方程式为______.
[实验结论]无水硫酸铜受热分解不仅仅生成Cu和SO3.
[反思与评价]
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素______(任写2点)
查看习题详情和答案>>
Ⅰ.某学习小组对粗铜提纯(电解精炼)后的阳极泥(主要成分为银、金)进行如下实验.

(1)操作③所需的仪器有:烧杯、______.
(2)为了回收金,他们查阅了有关资料如表:
| 编号 | 常温下反应 | 化学平衡常数 |
| 反应1 | Au+6HNO3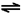 Au(NO3)3+3NO2↑+3H2O |
<10-5 |
| 反应2 | Au3++Cl- 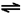 [AuCl4]- |
>105 |
Ⅱ.学习小组对无水硫酸铜分解的产物进行实验探究.
[提出问题]碳酸钙受热分解生成CaO和CO2,那么无水硫酸铜受热分解也只生成CuO和SO3吗?
[设计实验]按如图装置进行试验.

[实验过程]
a.准确称取无水硫酸铜2.40g于装置A试管中加热,直至固体全部变为黑色,经验证该黑色粉末为CuO
b.实验中,观察到装置E中的水部分被排入量筒中;实验结束后,测得量筒中水的体积为112mL(已折算成标准状态下气体的体积),并测得干燥管D的质量增加了1.32g.
(3)装置C的作用______.
(4)根据装置E、F中现象,推测还有气体______(填分子式)生成;实验生成的SO3为______ mol.
(5)装置A中反应的化学方程式为______.
[实验结论]无水硫酸铜受热分解不仅仅生成Cu和SO3.
[反思与评价]
(6)任何实验都存在误差,请指出本实验中可能造成误差的因素______(任写2点)