摘要:Mg(OH)2与Al(OH)3的比较 Mg(OH)2 Al(OH)3 物理 性质 均为白色固体.不溶于水 化 学 性 质 不稳定性 Mg(OH)2=MgO+ H2O 不稳定性 2Al(OH)3=Al2O3+3H2O 碱性 Mg(OH)2+2H+=Mg2++H2O 两性Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH-=AlO2-+2H2O 制 备 Mg2++2OH-= Mg(OH)2↓ Mg2++2NH3·H2O =Mg(OH)2↓+2NH4+ Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 不用强碱 AlO2-+CO2+2H2O= Al(OH)3↓+HCO3- 不用强酸
网址:http://m.1010jiajiao.com/timu3_id_50997[举报]
Al(OH)3和Mg(OH)2的分解温度是200~300℃和340~ 490℃,与聚乙烯的分解温度比较接近,将上述两种氢氧化物添加于聚乙烯制品中可以起阻燃作用的原理解释不正确的是
[ ]
A.两种氢氧化物受热分解吸热,防止制品温度上升
B.分解产生的水蒸气可以稀释可燃性气体,使之不易燃烧
C.分解形成的氧化物覆盖于制品上,阻止燃烧
D.两种氢氧化物受热难分解,阻止燃烧
查看习题详情和答案>>
B.分解产生的水蒸气可以稀释可燃性气体,使之不易燃烧
C.分解形成的氧化物覆盖于制品上,阻止燃烧
D.两种氢氧化物受热难分解,阻止燃烧
已知Mg(OH)2和Al(OH)3是工业上常用的阻燃剂,它们的热化学方程式分别为: Mg(OH)2(s)==MgO(s)+H2O(g); △H1=+81.5kJ·mol-1
Al(OH)3(s)=![]() Al2O3(s)+
Al2O3(s)+![]() H2O(g); △H2=+87.7kJ·mol-1
H2O(g); △H2=+87.7kJ·mol-1
下列说法正确的是 ( )
A.Mg(OH)2和Al(OH)3都是不溶于水的物质,所以可作工业阻燃剂。
B.等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好。
C.Mg(OH)2的碱性比Al(OH)3强,可推断金属性Al比Mg强。
D.Mg(OH)2和Al(OH)3作工业阻燃剂与它们分解产物都是耐高温材料无关。
查看习题详情和答案>>已知Mg(OH)2和Al(OH)3是工业上常用的阻燃剂,它们的热化学方程式分别为: Mg(OH)2(s)==MgO(s)+H2O(g); △H1=+81.5kJ·mol-1
Al(OH)3(s)=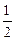 Al2O3(s)+
Al2O3(s)+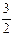 H2O(g); △H2=+87.7kJ·mol-1
H2O(g); △H2=+87.7kJ·mol-1
下列说法正确的是 ( )
Al(OH)3(s)=
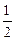 Al2O3(s)+
Al2O3(s)+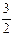 H2O(g); △H2=+87.7kJ·mol-1
H2O(g); △H2=+87.7kJ·mol-1下列说法正确的是 ( )
| A.Mg(OH)2和Al(OH)3都是不溶于水的物质,所以可作工业阻燃剂。 |
| B.等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好。 |
| C.Mg(OH)2的碱性比Al(OH)3强,可推断金属性Al比Mg强。 |
| D.Mg(OH)2和Al(OH)3作工业阻燃剂与它们分解产物都是耐高温材料无关。 |
已知Mg(OH)2和Al(OH)3是工业上常用的阻燃剂,Mg(OH)2的分解温度范围为340~490 ℃,氢氧化铝的分解温度范围为190~230 ℃,它们的热化学方程式分别为:
Mg(OH)2(s)=MgO(s)+H2O(g) ΔH1=+81.5 kJ·mol-1
Al(OH)3(s)=1/2Al2O3(s)+3/2H2O(g) ΔH2=+87.7 kJ·mol-1
下列说法不正确的是
Mg(OH)2(s)=MgO(s)+H2O(g) ΔH1=+81.5 kJ·mol-1
Al(OH)3(s)=1/2Al2O3(s)+3/2H2O(g) ΔH2=+87.7 kJ·mol-1
下列说法不正确的是
[ ]
A.Mg(OH)2和Al(OH)3高温下不分解,所以可做工业阻燃剂
B.等质量Mg(OH)2和Al(OH)3相比,Mg(OH)2阻燃效果较好
C.Mg(OH)2比Al(OH)3热稳定性高
D.Mg(OH)2和Al(OH)3作为工业阻燃剂与它们分解吸热及生成物具有耐高温性有关
查看习题详情和答案>>
B.等质量Mg(OH)2和Al(OH)3相比,Mg(OH)2阻燃效果较好
C.Mg(OH)2比Al(OH)3热稳定性高
D.Mg(OH)2和Al(OH)3作为工业阻燃剂与它们分解吸热及生成物具有耐高温性有关
(2013?安徽模拟)废易拉罐的成分比较复杂,据查,铝易拉罐各部分成分及含量(质量百分含量)见表:
为了验证罐身的组成成分,进行了如下实验:
【实验仪器与药品】
仪器:酒精灯、烧杯、试管、试管夹、漏斗、滤纸、铁圈、玻璃棒、砂纸、剪刀
药品:易拉罐、去污粉、NaOH溶液、KSCN溶液、盐酸、镁试剂、高碘酸(H5IO6,弱酸)
【实验方案】
实验预处理.将剪好的易拉罐片用砂纸打磨,除去表面的涂料层,直到光亮后用去污粉清洗干净备用.
【实验过程】分别向试管a、b中加入少量上述易拉罐片,进行如下操作:

请填写下列空白:
(1)图中操作①②所用到的玻璃仪器有
(2)沉淀A的成分为
(3)操作③观察到的现象为
反应的离子方程式为
(4)若试管a、b中取样相同,则分别加入足量的NaOH溶液、稀盐酸后,相同条件下理论上产生的气体体积V(a)
查看习题详情和答案>>
| Si | Fe | Cu | Mn | Mg | Cr | Zn | Ti | Al | |
| 罐身/% | 0.3 | 0.7 | 0.25 | 0.25 | 1.0~1.5 | - | - | - | 其余 |
| 罐盖/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 4.0~5.0 | - | 0.1 | 0.25 | 其余 |
| 拉环/% | 0.2 | 0.35 | 0.15 | 0.2~0.5 | 3.0~4.0 | 0.1 | 0.25 | 0.1 | 其余 |
【实验仪器与药品】
仪器:酒精灯、烧杯、试管、试管夹、漏斗、滤纸、铁圈、玻璃棒、砂纸、剪刀
药品:易拉罐、去污粉、NaOH溶液、KSCN溶液、盐酸、镁试剂、高碘酸(H5IO6,弱酸)
【实验方案】
实验预处理.将剪好的易拉罐片用砂纸打磨,除去表面的涂料层,直到光亮后用去污粉清洗干净备用.
【实验过程】分别向试管a、b中加入少量上述易拉罐片,进行如下操作:

请填写下列空白:
(1)图中操作①②所用到的玻璃仪器有
漏斗、烧杯、玻璃棒
漏斗、烧杯、玻璃棒
.(2)沉淀A的成分为
Fe、Cu、Mn、Mg等
Fe、Cu、Mn、Mg等
.(3)操作③观察到的现象为
开始生成白色沉淀,并逐渐增多,后沉淀部分溶解
开始生成白色沉淀,并逐渐增多,后沉淀部分溶解
;反应的离子方程式为
H++AlO2-+H2O═Al(OH)3↓
H++AlO2-+H2O═Al(OH)3↓
、2H++SiO32-═H2SiO3↓
2H++SiO32-═H2SiO3↓
、Al(OH)3+3H+═Al3++3H2O
Al(OH)3+3H+═Al3++3H2O
.(4)若试管a、b中取样相同,则分别加入足量的NaOH溶液、稀盐酸后,相同条件下理论上产生的气体体积V(a)
<
<
V(b)(填“<”、“>”或“=”).