网址:http://m.1010jiajiao.com/timu3_id_49566[举报]
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,分别与物质的量浓度相同,体积相同的三份AgNO3溶液恰好反应,用去的三种溶液的体积比为( )
| A.1:2:3 | B.6:3:2 | C.3:2:1 | D.1:1:1 |
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,分别与物质的量浓度相同,体积相同的三份AgNO3溶液恰好反应,用去的三种溶液的体积比为( )
A.1:2:3 B.6:3:2 C.3:2:1 D.1:1:1
查看习题详情和答案>>
一定温度下,下列叙述不能作为可逆反应A(g)+3B(g)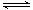 2C(g)达到平衡标志的是
2C(g)达到平衡标志的是
①恒压容器中,混合气体的密度保持不变;②单位时间内生成a mol A,同时消耗2a mol C
③A、B、C的浓度不再变化;④C的物质的量不再变化
⑤恒容容器中,混合气体的总压强不再变化;⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B;⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①②⑧ C.①②③ D.①⑤⑥
查看习题详情和答案>>
实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,反应如下:KHC8H4O4+NaOH=KNaC8H4O4+H2O.若氢氧化钠的溶液浓度为0.1 mol·L-1,到达终点时,溶液的PH约为9.1.
(1)为标定氢氧化钠溶液的浓度,准确称取一定质量的邻苯二甲酸氢钾加入250 ml锥形瓶中,用适量蒸馏水溶解,应选用________作指示剂,达到滴定终点时溶液由________色变为________色.
(2)在测定氢氧化钠溶液浓度时,有下列操作:①向溶液中加入1-2滴指示剂 ②向锥形瓶中加20 mL-30 mL蒸馏水溶解 ③用氢氧化钠溶液滴定到终点,半分钟不褪色 ④重复以上操作 ⑤准确称取0.4000 g-0.5000 g.苯二甲酸氢钾加入250 ml锥形瓶中 ⑥根据两次实验数据计算氢氧化钠的物质的量浓度.
以上各步中,正确的(填序号)操作顺序是___________
(3)上述操作中,将邻苯二甲酸氢钾直接放到锥形瓶中溶解,对实验是否有影响?________并说明理由:______________
(4)滴定前,用蒸馏水洗净碱式滴定管,然后加待测定的氢氧化钠溶液滴定,此操作使实验结果________(填“偏大”“偏小”或“无影响”)
(5)现准确称取KHC8H4O4(分子量204.2)晶体两份各为0.5105 g,分别溶于水后加入指示剂,用NaOH溶液滴定至终点,消耗NaOH溶液体积平均为20.00 mL,则NaOH溶液的浓度为________(结果保留四位有效数字).