摘要:答案:+3Cl2(g)=2PCl3(g) △H=-612kJ/mol (2)PCl5(g)=PCl3(g)+Cl2(g) △H=+93kJ/mol 25% 大于 (3)因为PCl5分解反应是吸热反应.温度太高.不利于PCl5的生成. (4)-399kJ/mol 等于 (5)PCl5+4H2O=H3PO4+5HCl
网址:http://m.1010jiajiao.com/timu3_id_47109[举报]
(2011?宣城二模)镁及其化合物在生产生活中有重要的作用.以水氯镁石(主要成分为MgCl2?6H2O)为原料生产碱式碳酸镁的主要流程如下:
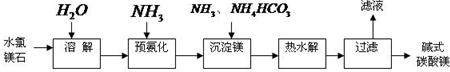
(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
(2)写出预氨化时发生的主要反应的离子方程式:
(3)沉淀镁时反应的温度不宜过高,原因是
(4)设计一个实验,确定产品碱式碳酸镁aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③
(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁.有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则.你同意该同学的想法吗?为什么?你的观点是
查看习题详情和答案>>

(1)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
NH4Cl
NH4Cl
.指出该物质在工农业生产中的一种用途:做氮肥(或其他合理答案)
做氮肥(或其他合理答案)
.(2)写出预氨化时发生的主要反应的离子方程式:
Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
Mg2++2NH3?H2O=Mg(OH)2↓+2NH4+
.(3)沉淀镁时反应的温度不宜过高,原因是
防止碳酸氢铵分解
防止碳酸氢铵分解
.(4)设计一个实验,确定产品碱式碳酸镁aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③
测出CO2的质量
测出CO2的质量
;④测出水蒸气的质量
测出水蒸气的质量
;⑤称量MgO.18.2g产品完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:a=3
3
;b=1
1
;c=3
3
.(5)从水氯镁石中可以提取无水氯化镁,电解熔融态的无水氯化镁可以得到金属镁.有同学认为:电解熔融的MgO也可制金属镁,在实际生产中可简化生产步骤,体现生产的简约性和经济性原则.你同意该同学的想法吗?为什么?你的观点是
不同意
不同意
.理由是因为MgO熔点很高,熔融时耗费大量的能量而增加生产成本
因为MgO熔点很高,熔融时耗费大量的能量而增加生产成本
.煤燃烧的反应热可通过以下两个途径来利用:
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳.然后使得到的氢气和一氧化碳在充足的空气中燃烧.
这两个过程的化学方程式为:
a.C(s)+O2(g)=CO2(g)△H=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g)△H=E2 ②
H2(g)+
O2(g)=H2O(g)△H=E3 ③
CO(g)+
O2(g)=CO2(g)△H=E4 ④
(1)途径b相比途径a有较多的优点,请写出其中一点:
(2)上述四个热化学方程式△H>0的是
(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为
查看习题详情和答案>>
a.利用煤在充足的空气中直接燃烧产生的反应热;
b.先使煤与水蒸气反应得到氢气和一氧化碳.然后使得到的氢气和一氧化碳在充足的空气中燃烧.
这两个过程的化学方程式为:
a.C(s)+O2(g)=CO2(g)△H=E1 ①
b.C(s)+H2O(g)=CO(g)+H2(g)△H=E2 ②
H2(g)+
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
(1)途径b相比途径a有较多的优点,请写出其中一点:
燃烧效率高(或其他合理答案)
燃烧效率高(或其他合理答案)
;(2)上述四个热化学方程式△H>0的是
②
②
(填写序号);(3)等质量的煤分别通过以上两条不同的途径产生的可利用的总能量关系正确的是
C
C
A.a比b多 B.a比b少 C.a与b在理论上相同
(4)根据能量守恒定律,E1、E2、E3、E4之间的关系为
E1=E2+E3+E4
E1=E2+E3+E4
.下列离子方程式书写不正确的是
A.NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时,
4OH- + 3SO2 = SO32-+ 2HSO3- + H2O
B.CuCl2溶液与Na2S溶液2:1反应,Cu2++ S2--= CuS↓
C.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,
2Fe2+ + 4Br- +3Cl2 = 2 Fe3+ + 2Br2 + 6Cl-
D. 1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:
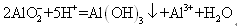
查看习题详情和答案>>
下列离子方程式书写不正确的是
| A.NaOH溶液与SO2反应,当n(NaOH):n(SO2)=4:3时,4OH- + 3SO2 = SO32-+ 2HSO3-+ H2O |
| B.CuCl2溶液与Na2S溶液2:1反应,Cu2++ S2--= CuS↓ |
| C.Cl2与FeBr2溶液反应,当n(Cl2):n(FeBr2)=1:1时,2Fe2+ + 4Br- +3Cl2 =" 2" Fe3+ + 2Br2 + 6Cl- |
D.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合: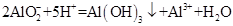 |