摘要:12.下列各组溶液之间的反应.所用离子方程式表示相同的是 A.硝酸钡与稀硫酸.氯化钡与硫酸钠 B.盐酸与碳酸钠.盐酸与碳酸氢钠 C.氢氧化钠与硫酸.氢氧化钡与硫酸 D.氢氧化钠与盐酸.氢氧化钾与醋酸
网址:http://m.1010jiajiao.com/timu3_id_426412[举报]
下列各组溶液之间的反应,所用离子方程式表示相同的是
A.硝酸钡与稀硫酸,氯化钡与硫酸钠
B.盐酸与碳酸钠,盐酸与碳酸氢钠
C.氢氧化钠与硫酸,氢氧化钡与硫酸
D.氢氧化钠与盐酸,氢氧化钾与醋酸
查看习题详情和答案>>下列各组溶液之间的反应,所用离子方程式表示相同的是( )
A.硝酸钡与稀硫酸,氯化钡与硫酸钠
B.盐酸与碳酸钠,盐酸与碳酸氢钠
C.氢氧化钠与硫酸,氢氧化钡与硫酸
D.氢氧化钠与盐酸,氢氧化钾与醋酸
查看习题详情和答案>>下列各组溶液之间的反应,所用离子方程式表示相同的是( )
| A.硝酸钡与稀硫酸,氯化钡与硫酸钠 |
| B.盐酸与碳酸钠,盐酸与碳酸氢钠 |
| C.氢氧化钠与硫酸,氢氧化钡与硫酸 |
| D.氢氧化钠与盐酸,氢氧化钾与醋酸 |
下列各组溶液之间的反应,所用离子方程式表示相同的是
- A.硝酸钡与稀硫酸,氯化钡与硫酸钠
- B.盐酸与碳酸钠,盐酸与碳酸氢钠
- C.氢氧化钠与硫酸,氢氧化钡与硫酸
- D.氢氧化钠与盐酸,氢氧化钾与醋酸
Ⅰ、下图表示各物质之间的转化关系。已知:常温下D、E、F、I、J为气体,其中E为黄绿色气体;H、I、J都为氧化物;B是一种常见的无色液体;M为红褐色固体。
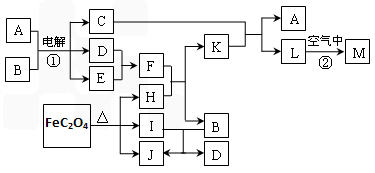
(1)反应①是重要的化学工业反应原理,写出其反应的离子方程式_____________________; (2)写出反应②的化学方程式______________。
(3)反应中FeC2O4生成H、I、J三种物质的物质的量相等,则J的电子式为________;
II、钛(Ti)被称为继铁、铝之后的第三金属,我国西南地区的钒钛磁铁矿储量十分丰富。如下图所示,将钛厂、甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。
(3)反应中FeC2O4生成H、I、J三种物质的物质的量相等,则J的电子式为________;
II、钛(Ti)被称为继铁、铝之后的第三金属,我国西南地区的钒钛磁铁矿储量十分丰富。如下图所示,将钛厂、甲醇厂组成产业链可以大大提高资源利用率,减少环境污染。
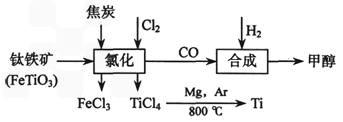
请填写下列空白:
(1)已知:
①Mg(s) +Cl2(g) = MgCl2(s);ΔH=-641 kJ/mol
②Ti(s)+2Cl2(g) = TiCl4(s);ΔH=-770 kJ/mol
则2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s);ΔH____________________
(2)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是_______________________________。写出钛铁矿在高温下经氯化法得到四氯化钛的化学方程式:_____________________。
查看习题详情和答案>>
(1)已知:
①Mg(s) +Cl2(g) = MgCl2(s);ΔH=-641 kJ/mol
②Ti(s)+2Cl2(g) = TiCl4(s);ΔH=-770 kJ/mol
则2Mg(s)+TiCl4(s)=2MgCl2(s)+Ti(s);ΔH____________________
(2)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。该电池中负极上的电极反应式是_______________________________。写出钛铁矿在高温下经氯化法得到四氯化钛的化学方程式:_____________________。