摘要:15.在浓CaCl2溶液中通入NH3和CO2.可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装置.请根据要求回答问题. (1)实验室制取.收集干燥的NH3.需选用上述仪器装置中的 . 若选用了C.D.则C中盛放的药品为 ,D的作用为 . (2)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时.应先通入的气体是 .写出制纳米级碳酸钙的化学方程式: . (3)试设计简单的实验方案.判断所得碳酸钙样品颗粒是否为纳米级. 答: .
网址:http://m.1010jiajiao.com/timu3_id_426219[举报]
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下图所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.

(1)实验室若用NH4Cl和熟石灰作试剂来制取、收集干燥的NH3,则需选用上述仪器装置中的
(2)若在A的分液漏斗内改加浓氨水,圆底烧瓶内加NaOH固体,也能制取氨气.请解释装置A中能产生氨气的原因
(3)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时,应先通入的气体是

写出制纳米级碳酸钙的化学方程式
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
查看习题详情和答案>>

(1)实验室若用NH4Cl和熟石灰作试剂来制取、收集干燥的NH3,则需选用上述仪器装置中的
BDE
BDE
(填装置序号).若要制取、收集干燥的CO2,请选择装置并按气流方向连接各仪器接口acdh
acdh
.(2)若在A的分液漏斗内改加浓氨水,圆底烧瓶内加NaOH固体,也能制取氨气.请解释装置A中能产生氨气的原因
氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出
氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠吸水,促使氨放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出
.(3)向浓CaCl2溶液中通入NH3和CO2气制纳米级碳酸钙时,应先通入的气体是
NH3
NH3
,若实验过程中有氨气逸出,应选用下列b
b
装置回收(填代号).
写出制纳米级碳酸钙的化学方程式
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
.(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
.在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间).下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.

(1)写出实验室制取NH3的化学方程式
(2)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接
(3)用图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用(选填字母编号);
A.碱石灰 B.生石灰 C.无水氯化钙
D.无水硫酸铜 E.烧碱
(4)向浓CaCl2溶液中通入NH3和C02气体制纳米级碳酸钙时,应先通入的气体是
(5)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
查看习题详情和答案>>

(1)写出实验室制取NH3的化学方程式
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O
| ||
2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+H2O
.
| ||
(2)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接
d
d
,e
e
接g
g
,f
f
接h;
(3)用图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用(选填字母编号);
A.碱石灰 B.生石灰 C.无水氯化钙
D.无水硫酸铜 E.烧碱
(4)向浓CaCl2溶液中通入NH3和C02气体制纳米级碳酸钙时,应先通入的气体是
NH3
NH3
,试写出制纳米级碳酸钙的化学方程式CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl
CaCl2+CO2+2NH3+H2O=CaCO3↓+2NH4Cl
;(5)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光照射,若出现一条光亮的通路,则是纳米级,否则不是
.
在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙.下面所示A-E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.
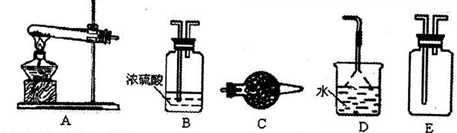
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的 .若选用了C、D,则C中盛放的药品为 ;D的作用为 .
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是 ,写出制纳米级碳酸钙的化学方程式 .
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级.答: .
查看习题详情和答案>>

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置中的
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是
(3)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级.答:
(12分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~10nm之间).下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题.
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选填字母):a接 , 接 , 接h;
(2)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入的气体是 ,试写出制纳米级碳酸钙的离子方程式 ;
(3)在浓CaCl2溶液和NH3用量正确的情况下,CO2不足或过量都会导致纳米级碳酸钙产量下降,若CO2过量溶液中大量存在的离子有(不考虑弱电解质的电离和盐类水解产生的少量离子)_____________________________,
(4)取反应后去除CaCO3的溶液分别做以下实验,下列实验判断合理的是:_________.
A.滴加少量Na2CO3溶液,若有沉淀说明CO2一定不足.
B.滴加少量盐酸,若有气泡,CO2一定过量.
C.测量溶液pH,若小于7,CO2一定过量
D.滴加少量BaCl2溶液,若无沉淀,CO2一定没有过量.
(5)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级 .
查看习题详情和答案>>