摘要:水的电离过程为H2OH++OH-.在25℃时水的离子积为KW=1.0×10-14.在35℃时水的离子积为KW=2.1×10-14.则下列叙述正确的是 ( ) A.c(H+)随着温度的升高而降低 B.35℃时c(H+)>c(OH-) C.35℃时的水比25℃时的水电离程度小 D.水的电离是个吸热过程
网址:http://m.1010jiajiao.com/timu3_id_425799[举报]
水的电离过程为H2O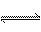 H++OH-,在不同温度下其离子积常数为KW(25 ℃)=1×10-14,KW(35 ℃)=2.1×10-14。则下列叙述正确的是( )
H++OH-,在不同温度下其离子积常数为KW(25 ℃)=1×10-14,KW(35 ℃)=2.1×10-14。则下列叙述正确的是( )
A.c(H+)随着温度的升高而降低 B.在35 ℃时,c(H+)>c(OH-)
C.水的电离程度:25 ℃>35 ℃ D.水的电离是吸热的
查看习题详情和答案>>
水的电离过程为H2O H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14, KW(35℃)=2.1×10-14。则下列叙述正确的是
H++OH-,在不同温度下其离子积为KW(25℃)=1.0×10-14, KW(35℃)=2.1×10-14。则下列叙述正确的是
| A.c(H+)随温度的升高而降低 | B.35℃时,c(H+)>c(OH-) |
| C.溶液:pH(35℃)>pH(25℃) | D.水的电离是吸热的过程 |
水的电离过程为H2O H+ + OH-,在不同温度下其离子积为:Kw(25℃)=1×10-14, Kw(35℃)=2.1 ×10-14。则下列叙述正确的是
H+ + OH-,在不同温度下其离子积为:Kw(25℃)=1×10-14, Kw(35℃)=2.1 ×10-14。则下列叙述正确的是
| A.c(H+)随着温度的升高而降低 | B.在35℃时,纯水中 c(H+) >c(OH-) |
| C.水的电离常数K(25℃)>K(35℃) | D.水的电离是一个吸热过程 |
 H+ + OH-,在不同温度下其离子积为:Kw(25℃)=1×10-14, Kw(35℃)=2.1 ×10-14。则下列叙述正确的是
H+ + OH-,在不同温度下其离子积为:Kw(25℃)=1×10-14, Kw(35℃)=2.1 ×10-14。则下列叙述正确的是 H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )
H++OH-,在25 ℃时水的离子积为KW=1.0×10-14,在35 ℃时水的离子积为KW=2.1×10-14,则下列叙述正确的是( )