摘要:6.下列离子方程式.一定正确的是C A.硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S↑ B.将标准状况下112 mL氯气通入10mL 1 mol/L的溴化亚铁溶液中: 2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- C.向磷酸二氢钾溶夜中加入过量的氢氧化钡溶液: 3Ba2++4OH-+2H2PO4-→Ba3(PO4)2↓+4H2O D.将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO
网址:http://m.1010jiajiao.com/timu3_id_425401[举报]
下列离子方程式,一定正确的是
A.硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S
B.纯碱溶液中滴加少量盐酸:CO32- + H+ → HCO3-
C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O
D.将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO
查看习题详情和答案>>
下列离子方程式,一定正确的是
A.硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S
B.纯碱溶液中滴加少量盐酸:CO32-+ H+ → HCO3-
C.过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O
D.将少量SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO
查看习题详情和答案>>
|
下列离子方程式,一定正确的是 | |
A. |
硫化亚铁与稀硝酸反应:FeS+2H+→Fe2++H2S |
B. |
将标准状况下112 mL氯气通入10 mL 1 mol/L的溴化亚铁溶液中:2Fe2++4Br-+3Cl2→2Fe3++2Br2+6Cl- |
C. |
过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO |
D. |
将少量 SO2气体通入Ca(ClO)2溶液中:SO2+Ca2++2ClO-+H2O→CaSO3↓+2HClO |
(16分)(1)下列有关实验操作或判断不正确的是 。
| A.配制一定物质的量浓度溶液,定容时俯视刻度线会导致所配溶液浓度偏小 |
| B.用干燥的pH试纸测定氯水的pH |
| C.配制稀硫酸时,可先在烧杯中加入一定体积的蒸馏水,再边缓慢加入浓硫酸边搅拌 |
| D.在天平左右两盘中各放一张白纸后,即可将NaOH固体放在白纸上称量 |
F.制备氢氧化亚铁时,将盛有NaOH溶液的滴管,伸入硫酸亚铁溶液中
(2)除杂(括号内为杂质):请把所加试剂和有关离子反应方程式填在空白处。
| | 试剂 | 离子反应方程式 |
| ①NaHCO3溶液(Na2CO3) | | |
| ② Fe2O3(Al2O3) | | |
| ③FeCl3溶液(FeCl2) | | |
| ④CO2(HCl) | | |
利用15N可以测定亚硝酸盐对地下水质的污染情况。
(1)下列说法正确的是________。
(2)15N的价层电子排布图为________;15NH4Cl的晶胞与CsCl相同,则15NH4Cl晶体中15NH4+的配位数为________;15NH4+中15N的杂化轨道类型为________。
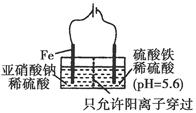
(3)工业上电解法处理亚硝酸盐的模拟工艺如图。已知阳极区发生化学反应:
2NO2—+8H++6Fe2+=N2↑+6Fe3++4H2O
①阳极电极反应方程式是________(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为_______
(填化学式);该现象表明c(H+)越大,H+氧化性越________;
③若电解时电路中有0.6 mol电子转移,且NaNO2有剩余,则电解池中生成Na2SO4________mol。
(1)下列说法正确的是________。
| A.14N与15N为同种核素 |
| B.14N的第一电离能小于14C |
| C.15NH3与14NH3均能形成分子间氢键 |
| D.CH315NH2与CH3CH214NH2互为同系物 |

(3)工业上电解法处理亚硝酸盐的模拟工艺如图。已知阳极区发生化学反应:
2NO2—+8H++6Fe2+=N2↑+6Fe3++4H2O
①阳极电极反应方程式是________(不考虑后续反应);
②若硫酸溶液浓度过大,阴极区会有气体逸出,该气体为_______
(填化学式);该现象表明c(H+)越大,H+氧化性越________;
③若电解时电路中有0.6 mol电子转移,且NaNO2有剩余,则电解池中生成Na2SO4________mol。