摘要:12.常温常压下.将a mol CO2气体通入1L 1 mol·L-1的NaOH溶液中.下列对所得溶液的描述不正确的是 A.当1/2<a <1时.所得溶液中存在: c(Na+) >c(CO32-)+ c(HCO3-)+ c(H2CO3) B.当a=1时.所得溶液中存在:c(OH-)+ c(CO32-)=c(H+)+ c(H2CO3) C.当a=1/2时.所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) D.当a=1时.所得溶液中存在:c(Na+) >c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
网址:http://m.1010jiajiao.com/timu3_id_424076[举报]
常温常压下,将a mol CO2气体通入1L 1 mol·L-1的NaOH溶液中,下列对所得溶液的描述不正确的是
A.当a=1/2时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
B.当1/2<a<1时,所得溶液中存在:c(Na+)>c(CO32-)+ c(HCO3-)+ c(H2CO3)
C.当a=1时,所得溶液中存在:c(OH-)+ c(CO32-)=c(H+)+ c(H2CO3)
D.当a=1时,所得溶液中存在:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
查看习题详情和答案>>
常温常压下,将a mol CO2气体通入1L 1 mol·L-1的NaOH溶液中,下列对所得溶液的描述不正确的是
A.当a=1/2时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
B.当1/2<a<1时,所得溶液中存在:c(Na+)>c(CO32-)+ c(HCO3-)+ c(H2CO3)
C.当a=1时,所得溶液中存在:c(OH-)+ c(CO32-)=c(H+)+ c(H2CO3)
D.当a=1时,所得溶液中存在:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
查看习题详情和答案>>常温常压下,将a mol CO2气体通入1L 1 mol·L-1的NaOH溶液中,下列对所得溶液的描述不正确的是
| A.当a=1/2时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+) |
| B.当1/2<a<1时,所得溶液中存在:c(Na+)>c(CO32-)+ c(HCO3-)+ c(H2CO3) |
| C.当a=1时,所得溶液中存在:c(OH-)+ c(CO32-)=c(H+)+ c(H2CO3) |
| D.当a=1时,所得溶液中存在:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
常温常压下,将a mol CO2气体通入1L 1 mol/L的NaOH溶液中,下列对所得溶液的描述不正确的是
- A.当a=0.5时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
- B.当0.5<a<1时,所得溶液中存在:c(Na+)>c(CO32-)+ c (HCO3-)+ c (H2CO3)
- C.当a=1时,所得溶液中存在:c(CO32-)+c(OH-)= c (H+)+ c (H2CO3)
- D.当a=1时,所得溶液中存在:c(Na+)> c (CO32-)>c(HCO3-)>c(OH-)>c(H+)
温室气体二氧化碳减排的一种方法是:从燃煤电厂或天然气电厂排放气中回收CO2,再与CH4热解炉产生的H2反应生成CH3OH.
CO2(g)+3H2(g)
CH3OH(g)+H2O(g)
(1)500℃时,在体积为1L的容积固定的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图1所示.
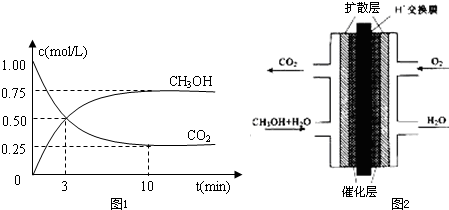
①从反应开始到平衡,氢气的平均反应速率v(H2)=______mol?L-1?min-1.
②该反应的平衡常数K=______(保留一位小数),平衡时H2的转化率为______.
③已知温度升高,K值减小.下列措施中能使
增大的是______.
A.升高温度B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离D.再充入1molCO2和3molH2
(2)CH3OH作为内燃机燃料或通过燃料电池驱动车辆.可减少CO2排放多达45%.
①已知:
CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1=+49.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则反应CH3OH(g)+
O2(g)═CO2(g)+2H2(g)的△H=______kJ?mol-1.
②甲醇质子交换膜燃料电池的结构示意图如图2,已知H+移向通入O2的电极,甲醇进入______极(填“正”或“负”),正极发生的电极反应为______.
查看习题详情和答案>>
CO2(g)+3H2(g)
| 一定条件 |
(1)500℃时,在体积为1L的容积固定的密闭容器中,充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化如图1所示.

①从反应开始到平衡,氢气的平均反应速率v(H2)=______mol?L-1?min-1.
②该反应的平衡常数K=______(保留一位小数),平衡时H2的转化率为______.
③已知温度升高,K值减小.下列措施中能使
| n(CH3OH) |
| n(CO2) |
A.升高温度B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离D.再充入1molCO2和3molH2
(2)CH3OH作为内燃机燃料或通过燃料电池驱动车辆.可减少CO2排放多达45%.
①已知:
CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H1=+49.0kJ?mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ?mol-1
则反应CH3OH(g)+
| 1 |
| 2 |
②甲醇质子交换膜燃料电池的结构示意图如图2,已知H+移向通入O2的电极,甲醇进入______极(填“正”或“负”),正极发生的电极反应为______.