摘要:氢气是中学化学中常见的气体之一.它是一种新型的绿色能源.又是一种重要的化工原料.试回答下列有关问题: (1)氢气燃烧热值很高.实验测得.在常温常压下.1 g H2完全完全燃烧生成液态水时放出142.9 kJ热量.则H2燃烧的热化学方程式为 . (2)某同学利用铁与硫酸反应制取氢气.实验时发现反应速率较慢.你认为可能的原因是 . a. H2SO4溶液太稀 b. H2SO4溶液太浓 c. 铁的纯度很高 d. 铁的纯度较小 (3)氢气是合成氨的重要原料.工业上合成氨的反应是N2 (g) + 3H2 (g)2NH3(g). ①一定条件下.一定量的N2和H2反应达到平衡后.改变某一外界条件.反应速率与时间的变化关系如图所示.其中加入催化剂的时刻是 . ②温度为T0C时.将2a mol H2和a mol N2放入恒容密闭容器中.充分反应达到平衡后测得N2的转化率与平衡混合物中的NH3的体积分数相等.则H2的转化率为 . (4)利用光分解水制氢是未来解决能源危机的理想方法之一.某研究机构设计了如图所示的砷化镓光电池系统实现分解水制氢. ①光电池的a极为 极,若电解池内电解液是硫酸钠溶液.则d极的电极反应式为 . ②上述装置中能量转化形式为 →电能→ .
网址:http://m.1010jiajiao.com/timu3_id_423757[举报]
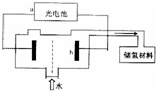 氢气是中学化学中常见的气体之一,它是一中新型的绿色能源,又是一种重要的化工原料.
氢气是中学化学中常见的气体之一,它是一中新型的绿色能源,又是一种重要的化工原料.(1)氢气燃烧热值高.实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出142.9kJ热量.则H2燃烧的热化学方程式为
(2)某同学利用铁与硫酸反应制取氢气,反应速率较慢,你认为可能的原因是:
(3)氢气是合成氨的重要原料.工业上合成氨的反应是:N2(g)+3H2(g)?2NH2(g)
①一定条件下,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如右图所示,其中加入催化剂引起反应速率变化的时间段是
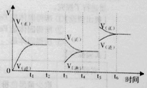
②温度为T℃时,将2a mol H2和 amolN2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则该温度下反应的平衡常数为
(4)利用光分解水制氢是未来解决能源危机的理想方法之一,某研究机构设计了如图的砷化镓光电池系统实现光分解水制氢.光电池的a极为
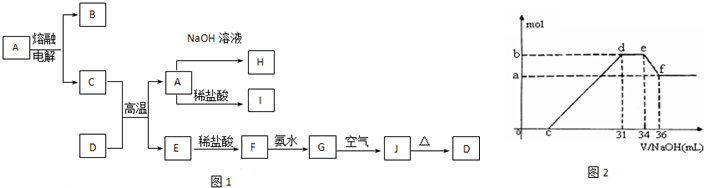
A-J是中学化学中常见的物质,它们之间的转化关系如框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.请回答下列问题:
(1)A的化学式为
(2)H溶液中通入过量的CO2,其反应的离子方程式是
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
上述现象说明溶液中
③b与a的差值为
查看习题详情和答案>>
(1)A的化学式为
Al2O3
Al2O3
(2)H溶液中通入过量的CO2,其反应的离子方程式是
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
[Al(OH)4]-+CO2═Al(OH)3↓+HCO3-
G→J的化学方程式为4Fe(OH)2+2H2O+O2═4Fe(OH)3
4Fe(OH)2+2H2O+O2═4Fe(OH)3
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因
Fe3++3H2O?Fe(OH)3+3H+
Fe3++3H2O?Fe(OH)3+3H+
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为
H++OH-=H2O
H++OH-=H2O
.②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式
NH4++OH-=NH3?H2O
NH4++OH-=NH3?H2O
;上述现象说明溶液中
H+
H+
结合OHˉ的能力最强(填离子符号).③b与a的差值为
0.008mol
0.008mol
mol.
A-J是中学化学中常见的物质,它们之间的转化关系如框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.请回答下列问题:
(1)A的化学式为______
(2)H溶液中通入过量的CO2,其反应的离子方程式是______G→J的化学方程式为______
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因______
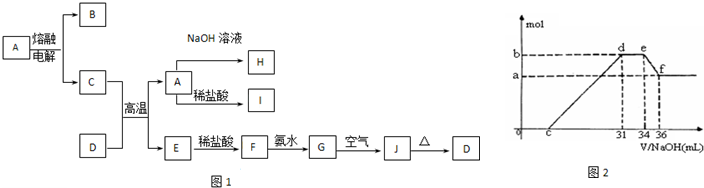
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为______.
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式______;
上述现象说明溶液中______结合OHˉ的能力最强(填离子符号).
③b与a的差值为______mol.
查看习题详情和答案>>
A-J是中学化学中常见的物质,它们之间的转化关系如框图1所示(部分产物已略去).已知A是一种高熔点物质,J是一种红褐色沉淀.请回答下列问题:
(1)A的化学式为______
(2)H溶液中通入过量的CO2,其反应的离子方程式是______G→J的化学方程式为______
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因______
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为______.
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式______;
上述现象说明溶液中______结合OHˉ的能力最强(填离子符号).
③b与a的差值为______mol.

查看习题详情和答案>>
(1)A的化学式为______
(2)H溶液中通入过量的CO2,其反应的离子方程式是______G→J的化学方程式为______
(3)D物质恰好溶于一定量的稀盐酸后,用合适的化学用语表示所得溶液显酸性的原因______
(4)实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低.某同学取一定量上述的C、E混合物 与一定量很稀的硝酸充分反应,反应过程中无气体放出.在反应结束后的溶液中,逐滴加入4mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示.试回答下列问题:
①图2中oc段没有沉淀生成,此阶段发生反应的离子方程式为______.
②在de段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式______;
上述现象说明溶液中______结合OHˉ的能力最强(填离子符号).
③b与a的差值为______mol.

查看习题详情和答案>>
中学化学常见部分元素原子结构及性质如表所示:
(1)①A元素在周期表中的位置为 .
②检验某溶液中含A的低价离子而不含其高价离子的方法是 .
(2)B与C形成的化合物的电子式为 .
(3)①F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的实验方法是 .
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则N的结构式为 .
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写) .
(5)(在25℃、101kPa下,已知D的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190.0kJ,该反应的热化学方程式是 .
查看习题详情和答案>>
| 序号 | 元素 | 结构及性质 |
| ① | A | A单质是生活中常见金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | B原子K、L、M层电子数之比是1:4:1 |
| ③ | C | C是活泼非金属元素,其单质常温下呈气态但化学性质稳定 |
| ④ | D | D单质被誉为“信息革命的催化剂”,是常用的半导体材料 |
| ⑤ | E | 通常情况下,E没有正化合价,A、C、F都能与E形成二种或二种以上化合物 |
| ⑥ | F | F元素的一种核素没有中子 |
②检验某溶液中含A的低价离子而不含其高价离子的方法是
(2)B与C形成的化合物的电子式为
(3)①F与E可以形成原子个数比分别为2:1、1:1的两种化合物X和Y,区别X与Y的实验方法是
②F与C组成的两种化合物M和N所含的电子数分别与X、Y相等,则N的结构式为
(4)有人认为B、D的单质用导线连接后插入NaOH溶液中可以形成原电池,你认为是否可以,若可以,试写出负极的电极方程式(若认为不行可不写)
(5)(在25℃、101kPa下,已知D的气态氢化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol电子放热190.0kJ,该反应的热化学方程式是