摘要:23.下表是实验室制备气体的有关内容: 编号 实验内容 实验原理 气体发生装置 ① 制氧气 H2O2→O2 ② 制氨气 NH4Cl→NH3 ③ 制氯气 HCl→Cl2 (1)上述气体中:从制备过程看.必须选择合适的氧化剂才能实现的是 ,从反应原理看.明显不同于其他两种气体的是 . (2)根据表中所列实验原理.从下列装置中选择合适的气体发生装置.将其编号填入上表中的空格中. (3)若用上述制备O2的装置制备NH..则选择的试剂为 . (4)制备C12需用8 mol·L-1的盐酸100mL.现用12 mol·L-1的盐酸来配制. ①为提高配制的精确度.量取浓盐酸的仪器可选用下列的 ②配制过程中.除上图所列仪器外.还需要的仪器有 . . . ③若标定所配盐酸的浓度是否准确.常采用的实验方法名称是 . (5)若用排空气法收集Cl2.在下列方框内画出气体收集装置图.
网址:http://m.1010jiajiao.com/timu3_id_421813[举报]
下表是实验室制备气体的有关内容:
(1)上述气体中:从制备过程看,必须选择合适的氧化剂才能实现的是
(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中.

(3)某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质:


①通入氯气后,A中的现象是
②C装置中发生反应的离子方程式为:
③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤):
(4)若用排空气法收集Cl2,在右边方框内画出气体收集装置图.
查看习题详情和答案>>
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | Ⅳ Ⅳ |
| ② | 制备氨气 | NH4Cl→NH3 | Ⅱ Ⅱ |
| ③ | 制备氯气 | HCl→Cl2 | Ⅰ或Ⅳ Ⅰ或Ⅳ |
Cl2
Cl2
(填气体的化学式,下同);从反应原理看,明显不同于其他两种气体的是NH3
NH3
.(2)根据表中所列实验原理,从下列装置中选择合适的气体发生装置,将其编号填入上表中的空格中.

(3)某学习小组设计了如下图实验,将氯气依次通过下列装置以验证氯气的性质:


①通入氯气后,A中的现象是
溶液变蓝色
溶液变蓝色
,整套实验装置存在的明显缺陷是无尾气吸收装置;
无尾气吸收装置;
.②C装置中发生反应的离子方程式为:
2Fe2++Cl2═2Fe3++2Cl-
2Fe2++Cl2═2Fe3++2Cl-
.③请你帮该小组同学设计一个实验,证明洗气瓶B中的Na2SO3已被氧化(简述实验步骤):
取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化
取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化
(4)若用排空气法收集Cl2,在右边方框内画出气体收集装置图.
下表是实验室制备气体的有关内容:
(1)上述气体制备中,从反应中有无电子转移的角度看,明显不同于其他气体的是
(2)若用上述制备O2的装置制备NH3,应选择的试剂为
(3)在浓CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是
(4)制备Cl2需用8mol?L-1的盐酸100ml,现用12mol?L-1的盐酸来配制.
①需要用量筒量取12mol?L-1的盐酸的体积为
②下列实验操作中,不正确的是
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
查看习题详情和答案>>
| 编号 | 实验内容 | 实验原理 |
| ① | 制氧气 | H2O2→O2 |
| ② | 制氨气 | NH4Cl→NH3 |
| ③ | 制氯气 | HCl→Cl2 |
②
②
(填编号),其实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl
CaCl2+2NH3+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3+2H2O
.
| ||
(2)若用上述制备O2的装置制备NH3,应选择的试剂为
浓氨水和氢氧化钠(或生石灰或碱石灰)
浓氨水和氢氧化钠(或生石灰或碱石灰)
.(3)在浓CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是
NH3
NH3
,试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是
. (4)制备Cl2需用8mol?L-1的盐酸100ml,现用12mol?L-1的盐酸来配制.
①需要用量筒量取12mol?L-1的盐酸的体积为
66.7
66.7
mL;②下列实验操作中,不正确的是
BC
BC
.A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
下表是实验室制备气体的有关内容:
(1)上述气体中,从反应中有无电子转移的角度看,明显不同于其他气体的是
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中.

(3)若用上述制备O2的装置制备NH3,应选择的试剂为
(4)在浓CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是
(5)制备Cl2需用8mol?L-1的盐酸100mL,现用12mol?L-1的盐酸来配制.
①需要用量筒量取12mol?L-1的盐酸的体积为
②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是
A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
查看习题详情和答案>>
| 编号 | 实验内容 | 实验原理 | 发生装置 |
| (1) | 制氧气 | H2O2→O2 | C C |
| (2) | 制氨气 | NH4Cl→NH3 | B B |
| (3) | 制氯气 | HCl→Cl2 | A或C A或C |
Cl2
Cl2
,写出实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl
CaCl2+2NH3+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3+2H2O
.
| ||
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中.

(3)若用上述制备O2的装置制备NH3,应选择的试剂为
浓氨水和氢氧化钠(或生石灰或碱石灰)
浓氨水和氢氧化钠(或生石灰或碱石灰)
.(4)在浓CaCl2溶液中通入NH3和CO2可以制得纳米级碳酸钙,制取时应先通入的气体是
NH3
NH3
,制取纳米级碳酸钙的化学方程式为CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
CaCl2+CO2+2NH3+H2O=CaCO3+2NH4Cl
.试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是
取少量样品和水混合形成分散系,用一束光从侧面照射,若出现光亮的通路,则证明样品是纳米级,否则不是
.(5)制备Cl2需用8mol?L-1的盐酸100mL,现用12mol?L-1的盐酸来配制.
①需要用量筒量取12mol?L-1的盐酸的体积为
66.7
66.7
mL;②实验室提供有如下仪器,为完成配制需要选择的仪器为(填序号)
ACFGH
ACFGH
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.100mL烧杯H.100mL容量瓶
③下列实验操作中.不正确的是
BC
BC
(填写标号).A.使用容量瓶前,检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C.配制溶液时,用量筒量取浓盐酸并沿玻璃棒倒入容量瓶中,缓慢加入蒸馏水到距离刻度线1~2cm处,改用胶头滴管滴加蒸馏水直到凹液面的最低点和刻度线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转和摇动多次.
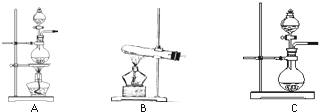 下表是实验室制备气体的有关内容:
下表是实验室制备气体的有关内容:| 编号 | 实验内容 | 实验原理 | 发生装置 |
| ① | 制氧气 | H2O2→O2 | C C |
| ② | 制氨气 | NH4Cl→NH3 | B B |
| ③ | 制氯气 | HCl→Cl2 | A或C A或C |
Cl2
Cl2
(填气体的化学式,下同.);从反应中有无电子转移的角度看,明显不同于其他气体的是NH3
NH3
,写出实验室制取该气体的化学方程式Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
(2)根据表中所列实验原理,从下列装置中选择合适的发生装置,将其编号填入上表的空格中.
(3)若用上述制备O2的装置制备NH3,则选择的试剂为
浓氨水和氢氧化钠(或生石灰等)
浓氨水和氢氧化钠(或生石灰等)
.(4)制备Cl2需用8mol?L-1的盐酸100mL,现用12mol?L-1的盐酸来配制.
①需要12mol?L-1的盐酸的体积为
66.7
66.7
mL(精确到0.1mL)②实验室提供有如下仪器,为完成配制需要选择的仪器为
ACFGH
ACFGH
.A. 100mL量筒 B.托盘天平 C.玻璃棒 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.100mL烧杯 H.100mL容量瓶
③在容量瓶的使用方法中,下列操作中,不正确的是
BC
BC
(填写标号).A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配溶液润洗
C. 配制溶液时用量筒量取浓盐酸后用玻璃棒引流入容量瓶中,缓慢加入蒸馏水到接近标线1cm~2cm处,用胶头滴管滴加蒸馏水直到凹液面的最低处和标线相平
D.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转和摇动多次
(5)若用排空气法收集Cl2,画出收集装置图.
下表是实验室制备气体的有关内容:
(1)上述气体中,从制备过程看,必须选择合适的氧化剂才能实现的是 (填气体的化学式);从反应原理看,明显不同于其它两种气体的是 (填气体的化学式);从收集方法来看,只能用一种方法收集的是 (填气体的化学式).
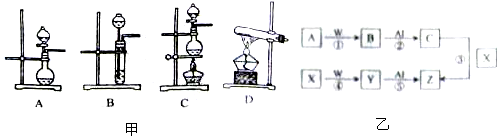
(2)根据表中所列实验原理,从图甲装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中.
(3)若用上述制备NH3的装置制备O2,则选择的试剂为 (填化学式);若用上述制备O2的装置制备
NH3,则选择的试剂的名称为 .
(4)若用排空气法收集Cl2,请画出气体收集装置图.
(5)有图乙所示无机物的转化关系,已知B和Y是上述三种气体中的两种.
a.当w为MnO2时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式.
b.当w为KMnO2时,反应①加热才能进行,反应④不加热就能进行,写出反应④的离子方程式. .
(6)已知Fe2++Br2=2Fe3++2Br-,现向100mL的FeBr2溶液中通入标准状况下Cl23.36L,充分反应后,测得溶液中Cl-与Br-的物质的量浓度相等(设通入Cl2前后溶液体积不变),则原FeBr2溶液中溶质的物质的量浓度为 .
 查看习题详情和答案>>
查看习题详情和答案>>
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制氧气 | H2O2→O2 | |
| ② | 制氨气 | NH4Cl→NH3 | |
| ③ | 制氯气 | HCl→Cl2 |
(2)根据表中所列实验原理,从图甲装置中选择合适的气体发生装置,将其选项填入表中相应编号的空格中.
(3)若用上述制备NH3的装置制备O2,则选择的试剂为
NH3,则选择的试剂的名称为
(4)若用排空气法收集Cl2,请画出气体收集装置图.
(5)有图乙所示无机物的转化关系,已知B和Y是上述三种气体中的两种.
a.当w为MnO2时,反应①不加热就能反应,反应④加热才能顺利进行,写出反应①的化学方程式.
b.当w为KMnO2时,反应①加热才能进行,反应④不加热就能进行,写出反应④的离子方程式.
(6)已知Fe2++Br2=2Fe3++2Br-,现向100mL的FeBr2溶液中通入标准状况下Cl23.36L,充分反应后,测得溶液中Cl-与Br-的物质的量浓度相等(设通入Cl2前后溶液体积不变),则原FeBr2溶液中溶质的物质的量浓度为
 查看习题详情和答案>>
查看习题详情和答案>>