摘要:解析:(1)阳极Fe为活性电极.反应为Fe-2e-===Fe2+.在阴极是H+放电生成H2. 反应为2H++2e-===H2↑. (2)阳极生成的Fe2+具有较强的还原性.易被酸性条件下的Cr2O氧化.反应为6Fe2 ++Cr2O+14H+===6Fe3++2Cr3++7H2O. (3)因在阴极H+放电.同时Cr2O氧化Fe2+时都要消耗H+.使溶液的pH上升. 促使Fe3+.Cr3+水解并最终完全转化为Cr(OH)3.Fe(OH)3沉淀. (4)若用Cu代替Fe电极.则Cu-2e-===Cu2+.但Cu2+无还原性.不能将Cr2O还 原. 答案:(1)Fe-2e-===Fe2+ 2H++2e-===H2↑ (2)6Fe2++Cr2O+14H+===6Fe3++2Cr3++7H2O (3)在阴极反应及Cr2O与Fe2+反应的过程中.将消耗大量的H+.使溶液pH上升. 促使Fe3+.Cr3+水解并最终转化为Fe(OH)3.Cr(OH)3沉淀 (4)不能 因为阳极产生的Cu2+不能使Cr2O还原到低价
网址:http://m.1010jiajiao.com/timu3_id_421416[举报]
阅读下列A、B、C、D、E、F六种短周期元素的相关信息。
①含A的物质焰色反应为黄色。
②B的原子最外层电子数是其内层电子数的3倍。
③C的最简单离子与Ne原子的电子数相同,且在具有相同电子数的简单离子中离子半径最小。
④D与B处于同主族。
⑤目前人类已知的物质(包括人工制造的物质)中,大多数都含有E元素。
⑥F元素的某种原子中只有质子,没有中子。
请根据上述信息回答下列问题:
(1)由已知六种元素中的三种组成的易溶于水的物质中,能促进水电离的物质是_____________(写出一种物质的化学式,下同),能抑制水电离的物质是____________。
(2)海水电源主要用于海上航标灯及相类似的海上用电设施,电源利用海水作电解液,空气中的氧作阴极活性物,C的单质作为阳极。写出这种海水电源的正极反应式:________________。
(3)常温下,向体积为1.5 L、浓度为0.1 mol/L的A 的最高价氧化物对应水化物的水溶液中通入2. 24L(标准状况)EB2气体,待反应充分后,溶液中各离子浓度由大到小的顺序是_________________。
(4)常温下,向c(H+) =1mol/L,c(Al3+)=c(Fe3+)= 0. 04 mol/L的溶液中加入A的最高价氧化物对应水化物的溶液,以调节溶液的pH(假设溶液体积不变)。那么最先析出的沉淀是___________(填写化学式),刚刚析出沉淀时溶液的pH=________。(已知Kap[Al(OH)3]=1.3×10-33mol4/L4,Ksp[Fe(OH)3]=2.6×10-39
mol4/L4)
查看习题详情和答案>>
①含A的物质焰色反应为黄色。
②B的原子最外层电子数是其内层电子数的3倍。
③C的最简单离子与Ne原子的电子数相同,且在具有相同电子数的简单离子中离子半径最小。
④D与B处于同主族。
⑤目前人类已知的物质(包括人工制造的物质)中,大多数都含有E元素。
⑥F元素的某种原子中只有质子,没有中子。
请根据上述信息回答下列问题:
(1)由已知六种元素中的三种组成的易溶于水的物质中,能促进水电离的物质是_____________(写出一种物质的化学式,下同),能抑制水电离的物质是____________。
(2)海水电源主要用于海上航标灯及相类似的海上用电设施,电源利用海水作电解液,空气中的氧作阴极活性物,C的单质作为阳极。写出这种海水电源的正极反应式:________________。
(3)常温下,向体积为1.5 L、浓度为0.1 mol/L的A 的最高价氧化物对应水化物的水溶液中通入2. 24L(标准状况)EB2气体,待反应充分后,溶液中各离子浓度由大到小的顺序是_________________。
(4)常温下,向c(H+) =1mol/L,c(Al3+)=c(Fe3+)= 0. 04 mol/L的溶液中加入A的最高价氧化物对应水化物的溶液,以调节溶液的pH(假设溶液体积不变)。那么最先析出的沉淀是___________(填写化学式),刚刚析出沉淀时溶液的pH=________。(已知Kap[Al(OH)3]=1.3×10-33mol4/L4,Ksp[Fe(OH)3]=2.6×10-39
mol4/L4)
(2008?广东)铜在自然界存在于多种矿石中,如:
①上表所列铜化合物中,铜的质量百分含量最高的是
②工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程会发生反应:2Cu2O+Cu2S
6Cu+SO2↑,反应的氧化剂是
③SO2尾气直接排放到大气中造成环境污染的后果是
④黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制.请简述粗铜电解得到精铜的原理:
⑤下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是
查看习题详情和答案>>
| 矿石名称 | 黄铜矿 | 斑铜矿 | 辉铜矿 | 孔雀石 |
| 主要成分 | CuFeS2 | Cu5FeS4 | Cu2S | CuCO3?Cu(OH)2 |
Cu2S
Cu2S
.②工业上以黄铜矿为原料.采用火法溶炼工艺生产铜.该工艺的中间过程会发生反应:2Cu2O+Cu2S
| ||
Cu2O,Cu2S
Cu2O,Cu2S
.③SO2尾气直接排放到大气中造成环境污染的后果是
二氧化硫是有毒气体,二氧化硫溶于水后形成酸性溶液,随雨水降下,就可能形成酸雨
二氧化硫是有毒气体,二氧化硫溶于水后形成酸性溶液,随雨水降下,就可能形成酸雨
;处理该尾气可得到有价值的化学品,写出其中1种酸和1种盐的名称硫酸,硫酸铵.
硫酸,硫酸铵.
.④黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制.请简述粗铜电解得到精铜的原理:
粗铜电解得到精铜的原理:电解池中,粗铜作阳极,精铜作阴极,电解质为硫酸铜溶液.阳极上发生氧化反应,Cu失去电子,使Cu单质变为Cu 2+进入溶液中Cu-e-═Cu 2+;阴极上发生还原反应,Cu 2+得到电子在阴极上析出Cu单质,Cu 2++e-═Cu,从而达到精制Cu的目的.
粗铜电解得到精铜的原理:电解池中,粗铜作阳极,精铜作阴极,电解质为硫酸铜溶液.阳极上发生氧化反应,Cu失去电子,使Cu单质变为Cu 2+进入溶液中Cu-e-═Cu 2+;阴极上发生还原反应,Cu 2+得到电子在阴极上析出Cu单质,Cu 2++e-═Cu,从而达到精制Cu的目的.
.⑤下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是
AD
AD
(填字母).| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铜绿的主成分是碱酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对;有 |
| B | 铜表易形成致密的氧化膜 | 铜容器可以盛放浓硫酸 | Ⅰ对;Ⅱ对;有 |
| C | 铁比铜活泼 | 例在铜板上的铁钉在潮湿空气中不易生锈 | Ⅰ对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | Ⅰ错;Ⅱ对;无 |
高纯铜(纯度可达99.99%)广泛应用于电器工业。某粗铜样品中含Fe、Ni、Ag、Au等四种金属杂质,可用电解法进行精炼制得高纯铜。
(1)请在下图1中标明电极材料和电解质溶液的名称
(1)请在下图1中标明电极材料和电解质溶液的名称
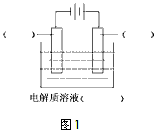
(2)已知Ni的金属活动性介于Fe和Sn之间。则精炼完成后,在阳极底部的沉积物中可回收到的金属为
__________(填化学式)。
(3)若在实验室中完成此实验,可用铅蓄电池做电源。铅蓄电池的电池总反应式为:
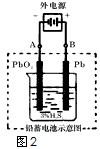
Pb+PbO2+4H++2SO42-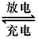 2PbSO4+2H2O,在完全放电耗尽PbO2和Pb时,若按上图2所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”)
2PbSO4+2H2O,在完全放电耗尽PbO2和Pb时,若按上图2所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”)
(4)电解完毕后,某兴趣小组欲对电解液中的离子进行分离,他们通过查阅资料,得知相关氢氧化物在不同pH下的溶解度曲线如图。
__________(填化学式)。
(3)若在实验室中完成此实验,可用铅蓄电池做电源。铅蓄电池的电池总反应式为:
Pb+PbO2+4H++2SO42-
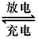 2PbSO4+2H2O,在完全放电耗尽PbO2和Pb时,若按上图2所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”)
2PbSO4+2H2O,在完全放电耗尽PbO2和Pb时,若按上图2所示连接进行充电,充电一段时间后,则在A电极上生成__________(填化学式),B电极上生成________(填化学式);充电完毕,铅蓄电池的正极是________极(填“A”或“B”) (4)电解完毕后,某兴趣小组欲对电解液中的离子进行分离,他们通过查阅资料,得知相关氢氧化物在不同pH下的溶解度曲线如图。
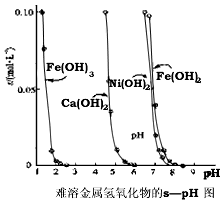
①结合上图分析,相同温度下Ksp[Cu(OH)2]、Ksp[Ni(OH)2]、Ksp[Fe(OH)2]由大到小的顺序为__________________________
②分离过程中,使上述溶液的pH逐渐增加,则溶液中的Cu2+、Fe3+和Ni2+沉淀的先后顺序依次为____________________。
查看习题详情和答案>>
②分离过程中,使上述溶液的pH逐渐增加,则溶液中的Cu2+、Fe3+和Ni2+沉淀的先后顺序依次为____________________。
 电解高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于废水和生活用水的处理.从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2NaOH+2H2O═Na2FeO4+H2↑.
电解高铁酸盐(如K2FeO4)是一种高效绿色氧化剂,可用于废水和生活用水的处理.从环境保护的角度看,制备高铁酸盐较好的方法为电解法:Fe+2NaOH+2H2O═Na2FeO4+H2↑.(1)采用铁片作阳极,NaOH溶液为电解质溶液,电解制备高铁酸钠,其电流效率可达到40%.写出阳极的电极反应式:
Fe-6e-+8OH-═FeO42-+4H2O
Fe-6e-+8OH-═FeO42-+4H2O
.(2)铁丝网电极是更理想的阳极材料,相同条件下,可将电流效率提高至70%以上,原因是
铁丝网的接触面积更大
铁丝网的接触面积更大
.研究亦发现,铁电极在某一电压范围内会生成Fe2O3膜而“钝化”,钝化的原因用反应式表示为因为铁电极上发生析氧反应4OH--4e-═O2↑+2H2O,氧气将铁氧化而得到氧化铁膜
因为铁电极上发生析氧反应4OH--4e-═O2↑+2H2O,氧气将铁氧化而得到氧化铁膜
.(3)FeO42-易与水反应生成絮状氢氧化铁,也会影响高铁酸盐的产率.若以铁丝网为阳极,在中间环节(对应图1中4h后)过滤掉氢氧化铁,合成过程中FeO42-浓度以及电流效率随时间的变化如图1中实线所示(图中曲线是每隔1h测得的数据).图中虚线部分对应于没有过滤氢氧化铁而连续电解的情况.下列判断正确的是
ACD
ACD
A.过滤掉氢氧化铁有利于获得较高浓度的高铁酸盐溶液
B.过滤掉氢氧化铁对电流效率影响不大
C.实验表明氢氧化铁的存在影响高铁酸盐浓度的增加
D.实验表明不过滤掉氢氧化铁,6h后电流效率几乎为0
(4)碱性条件下,高铁酸盐的稳定性与温度有关(如图2).随温度升高,高铁酸盐产率先增大后减小的原因是
升温电解一方面加快了高铁酸盐的生成速率,另一方面又加速FeO42-的分解
升温电解一方面加快了高铁酸盐的生成速率,另一方面又加速FeO42-的分解
.
(5)人们还对用铁的氧化物作电极制备高铁酸盐进行了研究,例如以磁铁矿多孔电极制备高铁酸盐,该研究方向的价值在于
BCD
BCD
A.将1mol Fe3O4氧化成高铁酸盐需10/3mol电子,可提高电流效率
B.以铁的氧化物为电极,可以实现变废(Fe3O4或铁锈)为宝(高铁酸盐)
C.自然界几乎没有铁单质,而有大量磁铁矿,该方法的原料来源广泛
D.磁铁矿作为多孔电极不会出现钝化现象.