摘要:27.如图所示.A.G.I均为单质.其中A.G为金属且都常被用作输电线.且G单质有特殊颜色.B为黑色粉末.L是由两种元素组成的盐.它是家庭厨房必备物品.请回答: (1)L的电子式为 (2)指出F在工业上的一种用途 (3)反应②的离子方程式为 (4)若利用反应④设计成原电池.其负极反应式为 (5)除反应⑤外.还有多种化学反应可由H生成K.下列物质能与H反应生成K的是 a.CO b.NaHCO c.NaHSO d.NaClO e.NHNO f.NH·HO (6)反应①中.当有4.0g B参加反应时.放出的热量为20.1kJ,则该反应的热化学方程式为
网址:http://m.1010jiajiao.com/timu3_id_419395[举报]
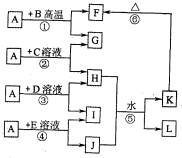 如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:(1)L的电子式为
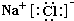
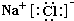
(2)指出F在工业上的一种用途
用作冶炼铝的原料或用作耐火材料
用作冶炼铝的原料或用作耐火材料
(3)反应②的离子方程式为
2Al+3Cu2+=2Al3++3Cu
2Al+3Cu2+=2Al3++3Cu
(4)若利用反应④设计成原电池,其负极反应式为
Al-3e-+4OH-=AlO2-+2H2O
Al-3e-+4OH-=AlO2-+2H2O
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是
bdf
bdf
(填选项字母)a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为
2Al(s)+3CuO(s)=Al2O3(s)+3Cu(s);△H=-1206kJ/mol
2Al(s)+3CuO(s)=Al2O3(s)+3Cu(s);△H=-1206kJ/mol
.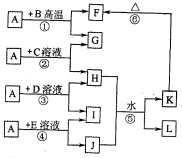 如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
(1)L的电子式为______
(2)指出F在工业上的一种用途______
(3)反应②的离子方程式为______
(4)若利用反应④设计成原电池,其负极反应式为______
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是______(填选项字母)
a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为______.
查看习题详情和答案>>
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
(1)L的电子式为______
(2)指出F在工业上的一种用途______
(3)反应②的离子方程式为______
(4)若利用反应④设计成原电池,其负极反应式为______
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是______(填选项字母)
a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为______.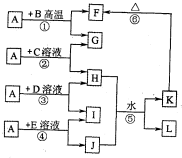
查看习题详情和答案>>
(1)L的电子式为______
(2)指出F在工业上的一种用途______
(3)反应②的离子方程式为______
(4)若利用反应④设计成原电池,其负极反应式为______
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是______(填选项字母)
a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为______.

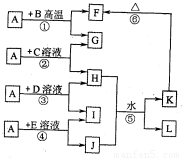
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电线,且G单质有特殊颜色,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
(1)L的电子式为______
(2)指出F在工业上的一种用途______
(3)反应②的离子方程式为______
(4)若利用反应④设计成原电池,其负极反应式为______
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是______(填选项字母)
a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
(1)L的电子式为______
(2)指出F在工业上的一种用途______
(3)反应②的离子方程式为______
(4)若利用反应④设计成原电池,其负极反应式为______
(5)除反应⑤外,还有多种化学反应可由H生成K.下列物质能与H反应生成K的是______(填选项字母)
a.CO2 b.NaHCO3 c.NaHSO4 d.NaClO e.NH4NO3 f.NH3?H2O
(6)反应①中,当有4.0g B参加反应时,放出的热量为20.1kJ,则该反应的热化学方程式为______.
 查看习题详情和答案>>
查看习题详情和答案>>
 (2012?洛阳二模)如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
(2012?洛阳二模)如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:(1)C的化学式为
CuCl2
CuCl2
.(2)指出F在工业上的一种用途
用作冶炼铝的原料,还可用作耐火材料
用作冶炼铝的原料,还可用作耐火材料
.(3)反应④的离子方程式为
2Al+2OH-+2H2O═2AlO2-+3H2↑
2Al+2OH-+2H2O═2AlO2-+3H2↑
.(4)除反应⑤外,还有多种化学反应可由H制备K.请写出一种反应的离子方程式
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
Al3++3NH3?H2O═Al(OH)3↓+3NH4+
.(5)L溶液与Pb(NO3)2溶液混合可形成沉淀,此沉淀的Ksp=1.6×10-5.将等体积的L溶液与Pb(NO3)2溶液混合,若L的浓度为0.1mol/L,则生成沉淀所需Pb(NO3)2溶液的最小浓度为
1.28×10-2
1.28×10-2
mol/L.