摘要: 配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3) Fe + HNO3 = Fe(NO3)3 + NO↑+ NO2↑+ H2O (2)此反应配平时可以有多组系数.其原因是 (3)请简述检验溶液中的金属阳离子的实验操作及现象
网址:http://m.1010jiajiao.com/timu3_id_417873[举报]
(1)配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3) Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O
(2)此反应配平时可以有多组系数,其原因是 (3)请简述检验溶液中的金属阳离子的实验操作及现象
(1)配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3)
![]() Fe +
Fe + ![]() HNO3 =
HNO3 =![]() Fe(NO3)3 +
Fe(NO3)3 +![]() NO↑+
NO↑+![]() NO2↑+
NO2↑+![]() H2O
H2O
(2)此反应配平时可以有多组系数,其原因是 (3)请简述检验溶液中的金属阳离子的实验操作及现象
查看习题详情和答案>>(1)配平下列反应的化学方程式(假定NO与NO2的物质的量之比为1:3)
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O
(2)此反应配平时可以有多组系数,其原因是 (3)请简述检验溶液中的金属阳离子的实验操作及现象
 Fe +
Fe +  HNO3 =
HNO3 = Fe(NO3)3 +
Fe(NO3)3 + NO↑+
NO↑+ NO2↑+
NO2↑+ H2O
H2O(2)此反应配平时可以有多组系数,其原因是 (3)请简述检验溶液中的金属阳离子的实验操作及现象
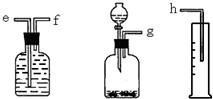
 (1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:
(1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:①用接口字母标出各仪器连接的顺序
g-f-e-h
g-f-e-h
量筒在实验中的作用是测量气体的体积
测量气体的体积
②有一块表面氧化成Na2O的金属钠,其质量为2.0g,实验后在量筒中收集到0.224L水,求样品中金属钠的质量分数是
23.0%
23.0%
.(假设在标准状况下测定)(2)(10分) HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+.AgNO2是一种难溶于水、易溶于酸的化合物.试回答下列问题:
①人体正常的血红蛋白含有Fe2+.若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒.下列叙述不正确的是
D
D
(填序号).A.亚硝酸盐被还原 B.维生素C具有还原性
C.维生素C将Fe3+还原为Fe2+D.在上述变化中亚硝酸盐是还原剂
②下列方法中,不能用来区分NaNO2和NaCl两种溶液的是
B
B
(填序号).A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI-淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
③某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:
NO2-+Cl2+H2O═NO3-+2H++2Cl-
NO2-+Cl2+H2O═NO3-+2H++2Cl-
.④Fe与过量稀硫酸反应可以制取FeSO4.若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
c
c
(填序号).a.Cl2 b.Fe c.H2O2 d.HNO3
⑤配平下列方程式:□Fe(NO3)3+□KOH□Cl2→□K2FeO4+□KNO3+□KCl+□H2O.
 (1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:
(1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合: