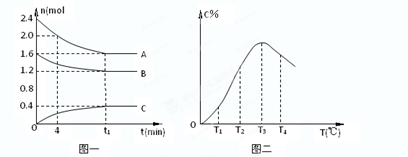
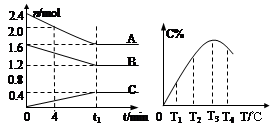摘要:10.在10L密闭容器中.A.B.C三种气态物质构成了可逆反应的体系.当在某一温度时.A.B.C物质的量与时间的关系如图1.C的百分含量与温度的关系如图2. 下列分析不正确的是 ( ) A.0-4分钟时.A的平均反应速率为0.02mol/ B.该反应的平衡常数表达式 C.由T1向T2变化时.V正 > V逆 D.此反应的正反应为放热反应
网址:http://m.1010jiajiao.com/timu3_id_417060[举报]
在10L密闭容器中,A、B、C三种气态物质构成可逆反应体系.某温度下,A、B、C三者物质的量与时间的关系如图1所示,而C的百分含量与温度的关系如图2所示.下列说法错误的是( )

查看习题详情和答案>>
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2.
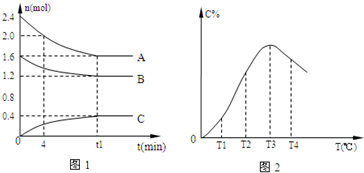
下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为放热反应 |