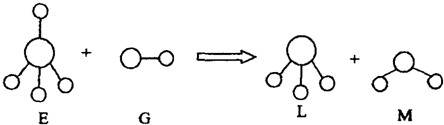
摘要:14.已知结构为正四面体型的离子A和直线型离子B反应.生成三角锥形分子C和V形分子D(组成A.B.C.D微粒的元素原子序数均小于10).下列说法正确的是 A.分子C与D不能发生化学反应 B.微粒A的空间结构与CH4相似.它们均为正四面体.所以它是非极性分子 C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S-H键 D.在25℃时.含有A的盐酸盐溶液的pH小于7
网址:http://m.1010jiajiao.com/timu3_id_416998[举报]
已知结构为正四面体型的离子A和直线型离子B反应,生成三角锥形分子C和V形分子D(组成A、B、C、D微粒的元素原子序数均小于10),下列说法正确的是
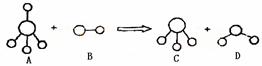
A.分子C与D不能发生化学反应
B.微粒A的空间结构与CH4相似,它们均为正四面体,所以它是非极性分子
C.固态D的熔沸点明显高于固态H2S的原因在于D分子中的共价键强于S-H键
D.在25℃时,含有A的盐酸盐溶液的pH小于7
查看习题详情和答案>>
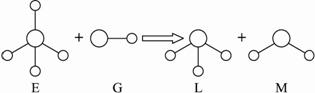
已知结构为正四面体型的离子E和直线型离子G反应,生成三角锥形分子L和V形分子M(组成E、G、L、M微粒的元素原子序数均小于10),反应过程用下图表示,则下列判断错误的是?
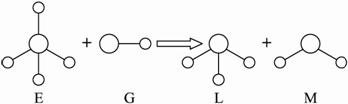
A.E、G、L、M都是10e-微粒?
B.L、M都是极性分子?
C.L能使紫色石蕊试液变蓝色?
D.E离子中质子数一定大于中子数
查看习题详情和答案>>