摘要:5.在化工生产中.要用到一种无色.可溶于水的晶体:铝铵矾.该晶体是一种复盐.其主要成分是十二水合硫酸铝铵.向该复盐的浓溶液中逐滴加入浓NaOH溶液.将发生一系列变化. NH4+ +Al3+ +H2O→Al(OH)3↓+NH3↑ 试回答: (1)硫酸铝铵在水溶液中的电离方程式为 , (2)在逐滴加入浓NaOH溶液的过程中.产生的现象有:①溶液中出现白色沉淀,②有刺激性气味的气体产生,③白色沉淀量逐渐增多,④白色沉淀完全消失,⑤白色沉淀量逐渐减少. 请答出各种现象由先到后出现的顺序 → → → → , (3)写出滴入NaOH溶液的过程中.有关反应的离子方程式:① ,② ,③ . 专题(八) 非金属元素答案 例1Ge:第Ⅳ主族元素.最高正价+4,最高价氧化物GeO2. Bi:第Ⅴ主族元素.最外层5个电子→满足8电子稳定结构应形成共价键数目:8-5=3→BiCl3→在BGO中铋为+3价→氧化物Bi2O3. 设BGO化学式为mGeO2·nBi2O3 有:2m=3n m∶n=3∶2 m=3 n=2 →BGO化学式为3GeO2·2Bi2O3 (或Bi4(GeO4)3) 例2答案:(1)H3PO4.5(3)O(O2与O3).P例3答案:(1)H2(2)2F2+2H2O→4HF+O2↑ (3)若D为N2.丙.丁分别是NH3和NO.在一定条件下可以反应(NH3.NO中N元素的化合价分别是-3.+2.0价居其中),若D为C.丙.丁分别是CH4与CO2.化合价分别是-4.+4.0价居其中.故理论上也可发生反应生成碳单质. 课堂练习 1A 2C 3C 4B 5D
网址:http://m.1010jiajiao.com/timu3_id_41667[举报]
在化工生产中,要用到一种无色、可溶于水的晶体:铝铵矾.该晶体是一种复盐,其主要成分是十二水合硫酸铝铵.向该复盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化.已知NH4+和AlO2-在水溶液中不能大量共存:
NH4++AlO2-+H2O=Al(OH)3↓+NH3↑
试回答:(1)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少.
请答出各种现象由先到后出现的顺序(用序号回答)
(2)写出滴入NaOH溶液的过程中,有关反应的离子方程式:①
查看习题详情和答案>>
NH4++AlO2-+H2O=Al(OH)3↓+NH3↑
试回答:(1)在逐滴加入浓NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体产生;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀量逐渐减少.
请答出各种现象由先到后出现的顺序(用序号回答)
①
①
→③
③
→②
②
→⑤
⑤
→④
④
;(2)写出滴入NaOH溶液的过程中,有关反应的离子方程式:①
Al3++3OH-=Al(OH)3↓
Al3++3OH-=Al(OH)3↓
②NH4++OH-=NH3↑+H2O
NH4++OH-=NH3↑+H2O
;③Al(OH)3+OH-=AlO2-+2H2O
Al(OH)3+OH-=AlO2-+2H2O
.
在化工生产中,要用到一种无色、易溶于水的晶体——铝铵矾,该晶体是一种复盐,其主要化学成分为十二水合硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化。已知NH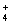 与AlO
与AlO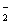 在水溶液中不能大量共存,会发生如下反应:NH
在水溶液中不能大量共存,会发生如下反应:NH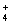 +AlO
+AlO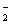 +H2O
+H2O Al(OH)3↓+NH3↑。试回答:
Al(OH)3↓+NH3↑。试回答:
(1)写出硫酸铝铵在水溶液中的电离方程式: 。?
若将硫酸铝铵溶液加入水稀释,物质的量浓度上升的离子是 (填离子符号)。?
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀?
②有刺激性气味的气体放出?
③白色沉淀量逐渐增多?
④白色沉淀完全消失
⑤白色沉淀逐渐减少
请排出以上各种现象由先到后出现的正确顺序 (用序号回答)。?
(3)请写出有关反应的离子方程式:
① 。?
② 。?
③ 。
查看习题详情和答案>>
在化工生产中,要用到一种无色、易溶于水的晶体――铝铵矾,该晶体是一种复盐,其主要成分为十二水硫酸铝铵[NH4Al(SO4)2?12H2O],向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列的变化,已知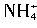 与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应:
与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应: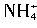 +[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答:
+[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答:
(1)写出硫酸铝铵在水溶液中的电离方程式:__________________________________。
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀逐渐减少。以上各种现象由先到后出现的顺序是_________________。
(3)请写出有关反应的离子方程式:①________,②______________, ③________________ 。 查看习题详情和答案>>
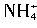 与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应:
与[Al(OH)4]-在水溶液中不能大量共存,会发生如下反应: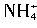 +[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答:
+[Al(OH)4]-=Al(OH)3↓+NH3↑+H2O。试回答:(1)写出硫酸铝铵在水溶液中的电离方程式:__________________________________。
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀逐渐减少。以上各种现象由先到后出现的顺序是_________________。
(3)请写出有关反应的离子方程式:①________,②______________, ③________________ 。 查看习题详情和答案>>
在化工生产中,要用到一种无色、易溶于水的晶体――铝铵矾,该晶体是一种复盐,其主要成分为十二水硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列的变化,已知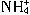 与Al
与Al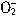 在水溶液中不能大量共存,会发生如下反应:
在水溶液中不能大量共存,会发生如下反应: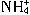 +Al
+Al +H2O=Al(OH)3↓+NH3↑。试回答:
+H2O=Al(OH)3↓+NH3↑。试回答:
(1)写出硫酸铝铵在水溶液中电离的方程式____________________________。
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀逐渐减少。请排出以上各种现象由先到后出现的正确顺序___________________。
(3)请写出有关反应的离子方程式:①_______________,
②__________________________,③____________________。 查看习题详情和答案>>
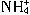 与Al
与Al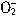 在水溶液中不能大量共存,会发生如下反应:
在水溶液中不能大量共存,会发生如下反应: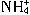 +Al
+Al +H2O=Al(OH)3↓+NH3↑。试回答:
+H2O=Al(OH)3↓+NH3↑。试回答:(1)写出硫酸铝铵在水溶液中电离的方程式____________________________。
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;④白色沉淀完全消失;⑤白色沉淀逐渐减少。请排出以上各种现象由先到后出现的正确顺序___________________。
(3)请写出有关反应的离子方程式:①_______________,
②__________________________,③____________________。 查看习题详情和答案>>
在化工生产中,要用到一种无色、易溶于水的晶体 铝铵矾,该晶体是一种复盐,其主要化学成分为十二水硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化,已知NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:
铝铵矾,该晶体是一种复盐,其主要化学成分为十二水硫酸铝铵,向该盐的浓溶液中逐滴加入浓NaOH溶液,将发生一系列变化,已知NH4+与AlO2-在水溶液中不能大量共存,会发生如下反应:
NH4++AlO2-+H2O=Al(OH)3↓+NH3↑;试回答:
(1)写出硫酸铝铵在水溶液中电离的方程式:________;若将硫酸铝铵溶液加入水稀释,物质的量浓度上升的离子是________(填离子符号)
(2)在逐滴加入NaOH溶液的过程中,产生的现象有:
①溶液中出现白色沉淀;②有刺激性气味的气体放出;③白色沉淀量逐渐增多;
④白色沉淀完全消失;⑤白色沉淀逐渐减少.请排出以上各种现象由先到后出现的正确顺序(用序号回答)________;
(3)请写出有关反应的离子方程式:
①________
②________
③________
查看习题详情和答案>>