摘要:已知A.B.C.D.E都是周期表中前四周期的元素.它们的核电荷数A<B<C<D<E.其中A.B.C是同一周期的非金属元素.化合物DC的晶体为离子晶体.D的二价阳离子与C的阴离子具有相同的电子层结构.AC2为非极性分子.B.C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高.E的原子序数为24.ECl3能与B.C的氢化物形成六配位的配合物.且两种配体的物质的量之比为2∶1.三个氯离子位于外界.请根据以上情况.回答下列问题:(答题时.A.B.C.D.E用所对应的元素符号表示) (1)A.B.C的第一电离能由小到大的顺序为 . (2)B的氢化物的分子空间构型是 .其中心原子采取 杂化. (3)写出化合物AC2的电子式 ,一种由B.C组成的化合物与AC2互为等电子体.其化学式为 . (4)E的核外电子排布式是 .ECl3形成的配合物的化学式为 . (5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时.B被还原到最低价.该反应的化学方程式是 .
网址:http://m.1010jiajiao.com/timu3_id_415943[举报]
 已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A原子的价电子层的p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素的原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素.回答下列问题:
已知A、B、C、D和E都是元素周期表中前20号的元素,它们的原子序数依次增大.A原子的价电子层的p轨道中只有1个电子;B、C、D元素的基态原子具有相同的能层数,B、D元素的原子的p能级上都有1个未成对电子,D原子得一个电子填入3p轨道后,3p轨道已充满,C原子的p轨道中有3个未成对电子;E是同周期第一电离能最小的元素.回答下列问题:(1)写出下列元素的符号:A
B
B
、BAl
Al
、CP
P
;(2)上述五种元素中最高价氧化物对应水化物酸性最强的是
HClO4
HClO4
,(填写化学式)碱性最强的是

(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
Cl
Cl
,电负性最大的元素是Cl
Cl
;(4)在AD3分子中A元素原子的原子轨道发生的是
sp2
sp2
杂化,分子空间构型为平面三角形
平面三角形
;(5)将B 的单质投入E的最高价氧化物对应水化物中,发生反应生成物中有此离子[B(OH)4]-离子方程式是
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑
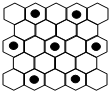
.(6)石墨具有平面层状结构,同一层中的原子构成许许多多的正六边形,它与熔融的E单质相互作用,形成某种青铜色的物质(其中的元素E用“●”表示),原子分布如图所示,该物质的化学式为
KC8
KC8
. (2012?梧州模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(2012?梧州模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增大.其中A原子核外有三个未成对电子;A与B可形成离子化合物B3A2;C元素是地壳中含量最高的金属元素;D原予核外的M层中有两对成对电子;E原子核外最外层只有1个电子,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)(1)E的核外电子排布式是
1s22s22p63s23p63d104s1
1s22s22p63s23p63d104s1
,A、B、C、D的第一电离能由小到大的顺序为Al<Mg<S<N
Al<Mg<S<N
.(2)B的氯化物的熔点远高于C的氯化物的熔点,理由是
氯化镁是离子晶体,氯化铝是分子晶体
氯化镁是离子晶体,氯化铝是分子晶体
;(3)A的最高价含氧酸根离子中,其中心原子采取
sp2
sp2
杂化,D的低价氧化物分子的空间构型是V形
V形
.(4)A、E形成某种化合物的晶胞结构如下图所示,则其化学式为
Cu3N
Cu3N
;(每个球均表示1个原子)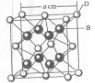 (2011?开封一模)[化学--选修物质结构与性质]
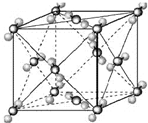
(2011?开封一模)[化学--选修物质结构与性质]已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大.A与其他4种元素既不在同一周期又不在同一主族.B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D和E属同一周期,又知E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,D跟B可形成离子化合物,其晶胞结构如图.请回答:
(1)A与c形成的共价化合物的分子式是
SiH4
SiH4
,杂化轨道是sp3
sp3
,分子的立体结构是正四面体
正四面体
.(2)B与C比较,电负性较小的是
Si
Si
(填元素符号);B与c形成的化合物晶体类型是分子晶体
分子晶体
. (3)E属元素周期表中第
四
四
周期,第ⅡB
ⅡB
族的元素,其元素名称是锌
锌
,它的+2价离子的电子排布式为1s22s22p63s2sp63d10
1s22s22p63s2sp63d10
.(4)从图中可以看出,D踉B形成的离子化合物的化学式为
CaF2
CaF2
;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是| 4×78/mol |
| a3cm3?6.02×1023mol-1 |
| 4×78/mol |
| a3cm3?6.02×1023mol-1 |
 (2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.
(2009?宿迁模拟)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E.其中B、D、E原子最外电子层的p能级(轨道)上的电子处于半满状态.通常情况下,A的一种氧化物分子为非极性分子,其晶胞结构如右下图所示.原子序数为31的元素镓(Ga)与元素B形成的一种化合物是继以C单质为代表的第一代半导体材料和GaE为代表的第二代半导体材料之后,在近10年迅速发展起来的第三代新型半导体材料.试回答下列问题:(答题时,A、B、C、D、E用所对应的元素符号表示)
(1)基态Ga原子的核外电子排布式为
1s22s22p63s23p63d104s24p1
1s22s22p63s23p63d104s24p1
.(2)A、B、C的第一电离能由大到小的顺序为
N>C>Si
N>C>Si
.(3)B元素的单质分子中有
2
2
个π键,与其互为等电子体的物质的化学式可能为CO(或其他合理答案)
CO(或其他合理答案)
(任写一种).(4)上述A的氧化物分子的中心原子采取
sp
sp
杂化,其晶胞中微粒间的作用力为范德华力
范德华力
.(5)EH3分子的空间构型为
三角锥形
三角锥形
,其沸点与BH3相比低
低
(填“高”或“低”),原因是NH3分子间能形成氢键,AsH3分子间不能形成氢键
NH3分子间能形成氢键,AsH3分子间不能形成氢键
.(6)向CuSO4溶液中逐滴加入BH3的水溶液,得到深蓝色的透明溶液.请写出该反应的离子方程式
Cu2++2NH3?H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
Cu2++2NH3?H2O=Cu(OH)2+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
. (2011?郑州二模)[化学--选修物质结构与性质]
(2011?郑州二模)[化学--选修物质结构与性质]已知A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次增大.B、C、D同周期,A、D同主族,B,C、D的最高价氧化物的水化物两两混合均能发生反应生成盐和水.E元素的原子核外共有20种不同运动状态的电子,且E的原子序数比D大4.
(1)B、C的第一电离能较大的是
Al
Al
(填元素符号).(2)A的氢化物的分子空间构型为
V型或折线型
V型或折线型
,其中心原子采取sp3
sp3
杂化.(3)A和D的氢化物中,沸点较高的是
H2O
H2O
(填化学式),其原因是水分子之间可以形成氢键,而H2S分子之间不能形成氢键
水分子之间可以形成氢键,而H2S分子之间不能形成氢键
.(4)仅由A与B元素组成,且含有非极性键的化合物是
Na2O2
Na2O2
(填化学式).(5)E的核外电子排布式是
1S22S22P63S23P64S2
1S22S22P63S23P64S2
.(6)B的最高价氧化物对应的水化物,其溶液与C单质反应的化学方程式是
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑或2Al+2NaOH+2H2O=2NaAlO2+3H2↑
2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑或2Al+2NaOH+2H2O=2NaAlO2+3H2↑
.(7)E单质在A单质中燃烧时得到一种白色晶体,其晶体的晶胞结构如右图所示,则该晶体的化学式为
CaO2
CaO2
.