摘要:(苏北四市2008--2009学年度高三年级第四次调研)已知A.B.C.D.E五种元素的原子序数依次递增.A.B.C.D位于前三周期.A位于周期表的s区.其原子中电子层数和未成对电子数相同,B的基态原子中电子占据三种能量不同的原子轨道.且每种轨道中的电子总数相同,D原子的核外成对电子数是未成对电子数的3倍.A.B.D三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体.A.B二种元素组成的原子个数比为1:1的化合物N是常见的有机溶剂.E有“生物金属 之称.E离子和氩原子的核外电子排布相同.请回答下列问题:(答题时.A.B.C.D.E用所对应的元素符号表示) (1)E的基态原子的外围电子排布式为 . (2)下列叙述正确的是 . a.M与水分子间能形成氢键.N是非极性分子 b.M和二氧化碳分子中的中心原子均采用sp2杂化 c.N分子中含有6个键和1个键 d.BD2晶体的熔点.沸点都比二氧化硅晶体的低 (3)E的一种氧化物Q.其晶胞结构如右上图所示.则Q的化学式为 .该晶体中氧的配位数为 . (4)电镀厂排放的废水中常含有剧毒的BC--离子.可在Q的催化下.先用NaClO将BC--氧化成BCD--.再在酸性条件下BCD--继续被NaClO氧化成C2和BD2. ① A.B.C.D四种元素的电负性由小到大的顺序为 . ② 与BCD--互为等电子体的分子.离子的化学式依次为 . ③ 上述反应中后一步反应的离子方程式是 . (5)在浓的ECl3的盐酸溶液中加入乙醚.并通入HCl至饱和.可得到配位数为6.组成为ECl3·6H20的绿色晶体.该晶体中两配体的物质的量之比为1:5.则该配离子的化学式为 .
网址:http://m.1010jiajiao.com/timu3_id_415936[举报]
已知A、B、C、D、E五种物质,且A、B、C、D的焰色反应呈黄色,它们的关系如下图所示,已知E为气体单质,能使带火星的木条复燃.

(1)写出下列物质的化学式:A
(2)写出A受热分解的化学方程式:
查看习题详情和答案>>

(1)写出下列物质的化学式:A
NaHCO3
NaHCO3
BNa2CO3
Na2CO3
CNa2O2
Na2O2
DNaOH
NaOH
EO2
O2
(2)写出A受热分解的化学方程式:
2NaHCO3
Na2CO3+CO2↑+H2O
| ||
2NaHCO3
Na2CO3+CO2↑+H2O
.
| ||
(2013?潍坊模拟)[化学--物质结构与性质]
已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子.
又知B、C和D是由两种元素的原子组成.请回答:
(1)组成A分子的原子的核外电子排布式是
(2)B和C的分子式分别是
(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成,则D分子中的中心原子的杂 化类型是
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2mol H2O,则E的分子式是
查看习题详情和答案>>
已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子.
又知B、C和D是由两种元素的原子组成.请回答:
(1)组成A分子的原子的核外电子排布式是
1s22s22p63s23p6
1s22s22p63s23p6
.(2)B和C的分子式分别是
HCl
HCl
和H2S
H2S
;C分子的立体结构呈V
V
形,该分子属于极性
极性
分子(填“极性”或“非极性”).(3)若向D的稀溶液中加入少量二氧化锰,有无色气体生成,则D分子中的中心原子的杂 化类型是
sp3
sp3
.(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2mol H2O,则E的分子式是
CH4O
CH4O
.(2008?珠海一模)已知A、B、C、D和E五种分子所含原子的数目依次为1、2、3、4和6,且都含有18个电子,又知B、C和D是由两种元素的原子组成,且D分子中两种原子个数比为1:1.
请回答:
(1)组成A分子的原子的核外电子排布式是
(2)B和C的分子式分别是
(3)向D的稀溶液中加入少量氯化铁溶液现象是
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2mol H2O,则E的分子式是
查看习题详情和答案>>
请回答:
(1)组成A分子的原子的核外电子排布式是
1s22s22p63s23p6
1s22s22p63s23p6
;(2)B和C的分子式分别是
HCl
HCl
和H2S
H2S
;C分子的空间构型为V
V
形,该分子属于极性
极性
分子(填“极性”或“非极性”);(3)向D的稀溶液中加入少量氯化铁溶液现象是
有气泡产生
有气泡产生
,该反应的化学方程式为2H2O2
2H2O+O2↑
| ||
2H2O2
2H2O+O2↑
;
| ||
(4)若将1mol E在氧气中完全燃烧,只生成1mol CO2和2mol H2O,则E的分子式是
CH4O
CH4O
.【物质结构与性质】
已知A、B、c、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3层电子且M层3d轨道电子全充满.
请回答下列问题:
(1)E元素基态原子的电子排布式为 .
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为 (填元素符号),其原因是 .
(3)D元素与氟元素相比,电负性:D F(填“>”、“=”或“<”),下列表述中能证明这一事实的是 (填选项序号)
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)离子化合物CA,的电子式为 ,它的晶体中含有多种化学键,但一定不含有的化学键是 (填选项序号).
A.极性键 B.非极性键C.配位键 D.金属键
(5)B2A4是重要的基本石油化工原料.B2A4分子中B原子轨道的杂化类型为 ;lmolB2A4分子中σ键 mol.
查看习题详情和答案>>
已知A、B、c、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子;E+原子核外有3层电子且M层3d轨道电子全充满.
请回答下列问题:
(1)E元素基态原子的电子排布式为
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为
(3)D元素与氟元素相比,电负性:D
A.常温下氟气的颜色比D单质的颜色深
B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态
D.比较两元素的单质与氢气化合时得电子的数目
(4)离子化合物CA,的电子式为
A.极性键 B.非极性键C.配位键 D.金属键
(5)B2A4是重要的基本石油化工原料.B2A4分子中B原子轨道的杂化类型为
[化学选修-物质结构与性质]
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
根据以上信息,回答下列问题:
(1)上述A、B、C、D四种元素中第一电离能最小的是 ,电负性最大的是 .(填相关元素的元素符号)
(2)A和D的氢化物中,沸点较高的是 (填相关物质的分子式);其原因是 .
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:
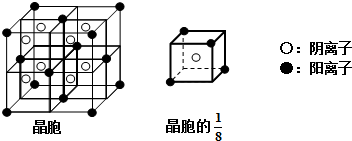
阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为 .
查看习题详情和答案>>
元素周期律是20世纪科学技术发展的重要理论依据之一.已知A、B、C、D、E五种元素都是元素周期表中前20号元素.A、B、C、D四种元素在元素周期表(长式)中的相对位置如下图所示,B、C、D的最高价氧化物的水化物两两混合,均能发生反应生成盐和水.E元素的原子序数均大于A、B、C、D元素,且不与A、B、C、D元素位于同主族.
| … | A | |||||
| B | C | D |
(1)上述A、B、C、D四种元素中第一电离能最小的是
(2)A和D的氢化物中,沸点较高的是
(3)A和E可组成离子化合物,其晶胞(在晶体中具有代表性的最小重复单元)结构如下图所示:

阳离子位于该正方体的顶点或面心;阴离子均位于小正方体中心.该化合物化学式为