摘要:11浓H2SO4和木炭在加热时发生反应的化学方程式是 2H2SO4(浓)+C CO2↑+2H2O+2SO2↑ 请从下图中选用所需的仪器组成一套进行该反应并要检出反应产物的装置.现提供浓H2SO4.木炭和酸性KMnO4溶液.其他固.液试剂自选.(连接和固定仪器所用的玻璃管.胶管.铁夹.铁架台及加热装置等均略去) 将所选的仪器连接顺序由上至下依次填入下表.并写出该仪器中应加试剂的名称及其作用. 选用的仪器 加入的试剂 作用 12实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙.大理石的主要杂质是氧化铁.以下是提纯大理石的实验步骤: (1)溶解大理石时.用硝酸而不同硫酸的原因是 , (2)操作Ⅱ的目的是 .溶液A是 , (3)写出检验滤液中是否含铁离子方程式: , (4)写出加入碳酸铵所发生反应的离子方程式: , 写出滤液B的一种用途: , (5)中一般含.试按下列提示完成含量分析的实验设计. 试剂:氢氧化钠标准溶液.盐酸标准溶液.酚酞 仪器:电子天平.锥形瓶.滴定管 实验步骤: ① ,②加入 ,③加入酚酞.用氢氧化钠标准溶液滴定. 13某学习小组探究浓.稀硝酸氧化性的相对强弱的.按下图装置进行试验.实验表明浓硝酸能将氧化成.而稀硝酸不能氧化.由此得出的结论是浓硝酸的氧化性强于稀硝酸. 可选药品:浓硝酸.3mo/L稀硝酸.蒸馏水.浓硫酸.氢氧化钠溶液及二氧化碳 已知:氢氧化钠溶液不与反应.能与反应 (1)实验应避免有害气体排放到空气中.装置③.④.⑥中乘放的药品依次是 , (2)滴加浓硝酸之前的操作时检验装置的气密性.加入药品.打开弹簧夹后 , (3)装置①中发生反应的化学方程式是 , (4)装置②的作用是 .发生反应的化学方程式是 , (5)该小组得出的结论的试验现象是 , (6)试验结束后.同学们发现装置①中溶液呈绿色.而不显蓝色.甲同学认为是该溶液中硝酸铜的质量分数较高所致.而乙同学认为是该溶液中溶解了生成的气体.同学们分别涉及了一下4个试验来判断两种看法是否正确.这些方案中可行的是 . a. 加热该绿色溶液.观察颜色变化 b. 加水稀释绿色溶液.观察颜色变化 c. 向该绿色溶液中通入氮气.观察颜色变化 d. 向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体.观察颜色变化 广东省增城中学2010届高三化学晚练
网址:http://m.1010jiajiao.com/timu3_id_415147[举报]
请从图1中选择所需装置,完成浓H2SO4和木炭在加热时的反应并检验反应产物(连接和固定仪器用的玻璃管、胶管、铁夹、铁架台及加热装置等均省略).
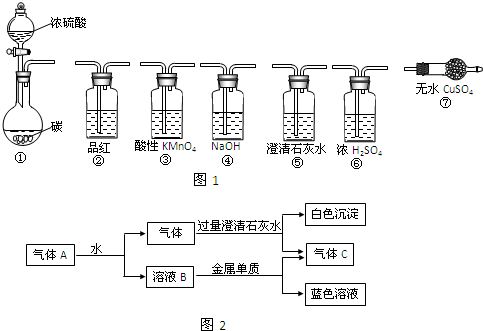
(1)浓H2SO4和木炭在加热时发生反应的化学方程式是:
(2)选用的实验装置和连接顺序是
(3)证明有CO2生成的实验现象是
(4)装置①也可以用于浓硝酸与木炭加热时发生反应,反应产生的气体产物A有如图2所示的变化.回答以下问题:
Ⅰ.气体C是
Ⅱ.B的稀溶液与金属单质反应生成蓝色溶液的离子方程式是:

标出电子转移的方向和总数.B在反应中表现
查看习题详情和答案>>

(1)浓H2SO4和木炭在加热时发生反应的化学方程式是:
2H2SO4(浓)+C
CO2↑+2H2O+2SO2↑
| ||
2H2SO4(浓)+C
CO2↑+2H2O+2SO2↑
.
| ||
(2)选用的实验装置和连接顺序是
①⑦②③⑤④
①⑦②③⑤④
(按从左至右连接顺序填装置序号).(3)证明有CO2生成的实验现象是
③中KMnO4溶液不褪色(或变浅),⑤中产生白色沉淀
③中KMnO4溶液不褪色(或变浅),⑤中产生白色沉淀
.(4)装置①也可以用于浓硝酸与木炭加热时发生反应,反应产生的气体产物A有如图2所示的变化.回答以下问题:
Ⅰ.气体C是
NO
NO
,溶液B中的溶质是HNO3
HNO3
(用化学式表示).Ⅱ.B的稀溶液与金属单质反应生成蓝色溶液的离子方程式是:


标出电子转移的方向和总数.B在反应中表现
氧化性和酸性
氧化性和酸性
. (2009?兖州市模拟)浓H2SO4和木炭在加热时发生反应的化学方程式是
(2009?兖州市模拟)浓H2SO4和木炭在加热时发生反应的化学方程式是2H2SO4(浓)+C
| ||
请从图中选择所需用的仪器(可重复选用)组成一套进行该反应并检出反应产物的装置.现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选.(连接和固定仪器用的玻璃管、胶管、铁管、铁架台及加热装置等均略去)将所选的仪器按连接顺序由上至下依次填入下表,并完成表格相应内容
| 所选用仪器的名称(填字母) | 加入的试剂名称 | 该装置作用 |
| 反应器(或发生气体) | ||
| 检出水 | ||
| 检出二氧化硫 | ||
| 酸性高锰酸钾溶液 | ||
| 检出二氧化碳 |
浓H2SO4和木炭在加热时发生反应的化学方程式是
2H2SO4(浓)+C
CO2↑+2H2O+2SO2↑
请从图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置.现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选.(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)
将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用.
查看习题详情和答案>>
2H2SO4(浓)+C
| ||
请从图中选用所需的仪器(可重复选用)组成一套进行该反应并要检出反应产物的装置.现提供浓H2SO4、木炭和酸性KMnO4溶液,其他固、液试剂自选.(连接和固定仪器所用的玻璃管、胶管、铁夹、铁架台及加热装置等均略去)

将所选的仪器连接顺序由上至下依次填入下表,并写出该仪器中应加试剂的名称及其作用.
| 选用的仪器 (填字母) |
加入的试剂 | 作用 |
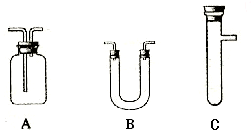
(1)有如图所示装置,为实现下列实验目的,其中y端适合于作入口的是

A 瓶内盛液体干燥剂,用以干燥气体
B 瓶内盛液体洗涤剂,用以除去某气体中的杂质
C 瓶内盛水,用以测量某难溶于水的气体的体积
D 瓶内贮存气体,加水时气体可被排出
E 收集密度比空气大的气体
F 收集密度比空气小的气体
(2)浓H2SO4和木炭在加热时发生反应的化学方程式是
填写下列空白.
①A中无水硫酸铜的作用
②证明SO2一定存在的现象是
③C中酸性KMnO4溶液的作用
④证明CO2一定存在的现象是
查看习题详情和答案>>
ABE
ABE
(多项)
A 瓶内盛液体干燥剂,用以干燥气体
B 瓶内盛液体洗涤剂,用以除去某气体中的杂质
C 瓶内盛水,用以测量某难溶于水的气体的体积
D 瓶内贮存气体,加水时气体可被排出
E 收集密度比空气大的气体
F 收集密度比空气小的气体
(2)浓H2SO4和木炭在加热时发生反应的化学方程式是
C+2H2SO4
CO2↑+2SO2↑+2H2O
| ||
C+2H2SO4
CO2↑+2SO2↑+2H2O
.图2中虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,
| ||
填写下列空白.
①A中无水硫酸铜的作用
检验水蒸气存在
检验水蒸气存在
.②证明SO2一定存在的现象是
B中品红退色
B中品红退色
.③C中酸性KMnO4溶液的作用
除去SO2
除去SO2
.④证明CO2一定存在的现象是
D中品红不退色,E中变浑浊
D中品红不退色,E中变浑浊
.