摘要:定容容器A与定压容器B的体积开始时相同.A中的SO2与O2的量分别与B中的相同.经一定时间在相同温度下达到平衡.有关叙述正确的是 A. A中混合气体的平均摩尔质量比B中的小 B. A中的反应速率比B中快 C. B中SO2的转化率比A中高 D.若A.B中皆再加入同量的氩气.平衡不移动 限时训练8
网址:http://m.1010jiajiao.com/timu3_id_415023[举报]
定容容器A与定压容器B的体积开始时相同,内皆装有同质量,同物质的量之比的SO2与O2混合气体,经一定时间在相同温度下达到平衡。有关叙述正确的是
[ ]
A.A、B中SO2的转化率相同
B.B中的反应速率比A中快
C.B中SO2的转化率比A中高
D.若A、B中皆再加入同量的氩气,平衡不移动
查看习题详情和答案>>
B.B中的反应速率比A中快
C.B中SO2的转化率比A中高
D.若A、B中皆再加入同量的氩气,平衡不移动
恒容容器甲与恒压容器乙开始时的体积相同,均盛有2 mol SO2和1 mol O2的混合气体,经一定时间反应,在相同温度下达到平衡,有关平衡时的叙述正确的是
A.甲、乙中SO2的体积分数相同
B.甲中的反应速率比乙中快
C.乙中SO2的转化率比甲中高
D.若甲、乙中皆再加入同量的氢气,平衡不移动
查看习题详情和答案>>在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g);测得CO2和CH3OH(g)的浓度随时间变化如图1所示.该反应过程中的能量变化如图2所示.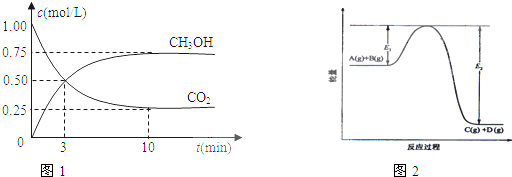
(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
(2)该反应的平衡常数表达式为
(3)如果在达平衡后某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡
a.向正反应方向移动 b.向逆反应方向移动 c.不移动 d.无法确定平衡移动方向
(4)下列措施中能使
增大的是
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
(5)在反应体系中加入催化剂,E1和E2的变化是:E1
查看习题详情和答案>>

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=
0.225
0.225
mol/(L?min).(2)该反应的平衡常数表达式为
K=
| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
K=
.该条件下的平衡常数K=| c(CH3OH)c(H2O) |
| c(CO2)c3(H2) |
5.33
5.33
(可用分数表示),温度升高,K值减少
减少
(填“增大”“不变”或者“减少”)(3)如果在达平衡后某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡
b
b
(填写序号).a.向正反应方向移动 b.向逆反应方向移动 c.不移动 d.无法确定平衡移动方向
(4)下列措施中能使
| n(CH3OH) |
| n(CO2) |
CD
CD
.A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
(5)在反应体系中加入催化剂,E1和E2的变化是:E1
减小
减小
,E2减小
减小
(填“增大”“减小、”“不变”).对反应热是否有影响?无
无
,原因是催化剂不能改变反应物的总能量与生成物总能量的差值,即反应热不变
催化剂不能改变反应物的总能量与生成物总能量的差值,即反应热不变
.(8分)在体积为2 L的密闭容器中,充入lmol CO2和2.6mol H2,一定条件下发生反应:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H= ―49.0 kJ?mol-1
CH3OH(g)+H2O(g) △H= ―49.0 kJ?mol-1
测得CO2和CH3OH(g)的浓度随时间变化如右图所示:
(1)从反应开始到第10 min,氢气的平均反应速率v(H2)= ,在这段时间内,反应放出的热量= 。
(2)在该条件下,反应的平衡常数K的值 = ,如果在某一时刻保持温度不变,只改变浓度,使c(CO2) =1.00 mol/L,c(H2) = 2.00 mol/L,c(CH3OH) = c(H2O) = 0.80 mol/L,则平衡 (填写序号)。
a.向正反应方向移动 b.向逆反应方向移动 c.不移动 d.无法确定平衡移动方向
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是 (填写序号)。
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入l mol CH3OH(g)
(4)在催化剂的作用下,CO2与H2能够合成许多物质,如甲醇、烃类、二甲醚等,但反应体系中若混入杂质,则反应很难进行,可能的原因是 。
查看习题详情和答案>>
在体积为1L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ
测得CO2和CH3OH(g)的浓度随时间变化如图所示:
(1)从反应开始到第10min,氢气的平均反应速率v(H2)=______,在这段时间内,反应放出的热量=______.
(2)在该条件下,反应的平衡常数K的值=______(保留2位小数),如果在某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡______(填写序号).
a.向正反应方向移动 b.向逆反应方向移动
c.不移动 d.无法确定平衡移动方向
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是______(填写序号).
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入1mol CH3OH(g)
(4)在催化剂的作用下,CO2与H2能够合成许多物质,如甲醇.烃类.二甲醚等,但反应体系中混入杂质,则反应很难进行,可能的原因是______.
 查看习题详情和答案>>
查看习题详情和答案>>
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ
测得CO2和CH3OH(g)的浓度随时间变化如图所示:
(1)从反应开始到第10min,氢气的平均反应速率v(H2)=______,在这段时间内,反应放出的热量=______.
(2)在该条件下,反应的平衡常数K的值=______(保留2位小数),如果在某一时刻保持温度不变,只改变浓度,使c(CO2)=1.00mol/L,c(H2)=0.40mol/L,c(CH3OH)=c(H2O)=0.80mol/L,则平衡______(填写序号).
a.向正反应方向移动 b.向逆反应方向移动
c.不移动 d.无法确定平衡移动方向
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是______(填写序号).
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离 d.再充入1mol CH3OH(g)
(4)在催化剂的作用下,CO2与H2能够合成许多物质,如甲醇.烃类.二甲醚等,但反应体系中混入杂质,则反应很难进行,可能的原因是______.
 查看习题详情和答案>>
查看习题详情和答案>>