摘要:15.(江苏省江浦高级中学高三化学2010第一轮复习模块检测)已知:4NH3(g) + 5O2 + 6H2O(g).△H = -1025kJ/mol.该反应是一个可逆反应.若反应物起始的物质的量相同.下列关于该反应的示意图不正确的是
网址:http://m.1010jiajiao.com/timu3_id_414854[举报]
已知反应4NH3+5O2?4NO+6H2O,若反应速率分别用v (NH3)、v (O2)、v (NO)、v (H2O)(mol?L-1?min-1)表示,则下列正确的关系是( )
(2010?南通模拟)下列框图涉及到的物质所含元素中,除一种元素外,其余均为短周期元素.已知:A、E为无气体单质,D为红色金属单质,B为黑色氧化物(部分反应的产物未列全).
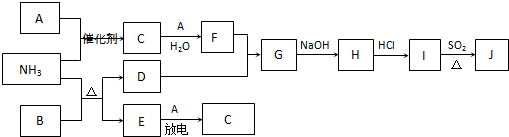
请回答下列问题:
(1)在NH3与F等物质的量反应后的溶液中,离子浓度由大到小的顺序为
(2)I、J是同种金属的氯化物,且J为白色沉淀.则SO2还原I生成J的离子方程式为
(3)汽车尾气中常含有C.NH3在加热和催化剂存在的条件下能消除C的污染.已知:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1
则NH3与C反应的热化学方程式为
(4)有人认为:“表面化学”研究成果能使NH3和C的反应在催化剂表面进行时的效率大大提高,从而使污染物D的转化率大大提高.请你应用化学基本理论对此观点进行评价:
查看习题详情和答案>>

请回答下列问题:
(1)在NH3与F等物质的量反应后的溶液中,离子浓度由大到小的顺序为
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
c(NO3-)>c(NH4+)>c(H+)>c(OH-)
.(2)I、J是同种金属的氯化物,且J为白色沉淀.则SO2还原I生成J的离子方程式为
2Cu2++2Cl-+SO2+2H2O═2CuCl↓+4H++SO42-
2Cu2++2Cl-+SO2+2H2O═2CuCl↓+4H++SO42-
.(3)汽车尾气中常含有C.NH3在加热和催化剂存在的条件下能消除C的污染.已知:
①4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905kJ?mol-1
②4NH3(g)+3O2(g)?2N2(g)+6H2O(g)△H=-1268kJ?mol-1
则NH3与C反应的热化学方程式为
6NO(g)+4NH3(g)═5N2(g)+6H2O(g)△H=-1812.5 kJ?mol-1
6NO(g)+4NH3(g)═5N2(g)+6H2O(g)△H=-1812.5 kJ?mol-1
.(4)有人认为:“表面化学”研究成果能使NH3和C的反应在催化剂表面进行时的效率大大提高,从而使污染物D的转化率大大提高.请你应用化学基本理论对此观点进行评价:
该研究只能提高化学反应速率,不能使化学平衡发生移动
该研究只能提高化学反应速率,不能使化学平衡发生移动
.(2012?惠州模拟)已知:4NH3(g)+5O2(g)=4NO(g)+6H2O(g),△H=-1025kJ/mol,该反应是一个可逆反应,若反应物起始的物质的量相同,下列关于该反应的示意图不正确的是( )
查看习题详情和答案>>
已知:4NH3+5O2
4NO+6H2O;4NO+3O2+2H2O→4HNO3
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空:
(1)amol NO完全转化为HNO3需要空气
(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为
(3)20.0moL的NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量的硝酸,以及其它成分.(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率.
查看习题详情和答案>>
| 一定条件 |
设空气中氧气的体积分数为0.20,氮气体积分数为0.80,请完成下列填空:
(1)amol NO完全转化为HNO3需要空气
3.75a
3.75a
mol;(2)为使NH3恰好完全氧化为一氧化氮,氨-空气混合物中氨的体积分数为
0.14
0.14
(保留2位小数).(3)20.0moL的NH3用空气氧化,产生混合物的组成为:NO 18.0mol、O2 12.0mol、N2 150.0mol和一定量的硝酸,以及其它成分.(高温下NO和O2不反应)计算氨转化为NO和HNO3的转化率.
已知反应4NH3+5O2?4NO+6H2O,若在反应开始后5s~10s之间的反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列判断正确的关系是( )
A、
| ||
B、
| ||
C、
| ||
D、
|