摘要:10.(江苏省赣榆一中2010届高三12月阶段考试化学)化合物 KxFe(C2O4)y· 3H2O 是一种光敏材料.实验室可以用如下的方法来制备这种材料并测定这种材料的组成. Ⅰ.制备 ( 1 )结晶时应将溶液用冰水冷却.这样操作的原因是 ( 2 )操作 a 的名称是 . Ⅱ.组成测定 称取一定质量的晶体置于锥形瓶中.加入足量的蒸馏水和稀 HZSO 4 .将 C2O42-转化为 H2C2O4后用 0 .1000 mol/LKMnO4溶液滴定.当消耗 KMnO4溶液 24.00mL 时恰好完全反应,再向溶液中加入适量的还原剂.恰好将 Fe3+完全转化为 Fe2+.用相同浓度的 KMnO4溶液继续滴定.当 Fe2+完全氧化时.用去 KMnO4溶液 4.00mL .第二次滴定的离子方程式为 (3)配制 100mL0.1000 mol/LKMnO4溶液及滴定实验中所需的玻璃仪器除烧杯.玻璃棒.胶头滴管.量筒.锥形瓶外还有 . ( 4)该化合物 KxFe(C2O4)y· 3H2O中x= ( 1 )用冰水冷却可降低KxFe(C2O4)y· 3H2O的溶解度.析出更多的晶体 MnO4-十 5Fe2+ + 8H+ ==Mn2++ 5Fe3+ + 4H2O ( 3 ) 100 mL 容量瓶.酸式滴定管
网址:http://m.1010jiajiao.com/timu3_id_414798[举报]
进入21世纪,我国的几大环境污染事件中,吉林石化双苯厂发生爆炸是唯一造成国际影响的事件,近100吨含有苯、甲苯、硝基苯和苯胺( 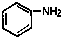 )等污染物的废水流入松花江,最终经俄罗斯入海.
)等污染物的废水流入松花江,最终经俄罗斯入海.
(1)写出上述四种污染物中含有的官能团的结构简式 ;
(2)苯、甲苯、硝基苯和苯胺4种物质的关系为 ;
A.同系物 B.同分异构体 C.芳香烃 D.芳香族化合物
(3)苯胺和NH3与酸反应的性质相似,写出苯胺与盐酸反应的离子方程式 ;
(4)①写出由苯制硝基苯的化学方程式 ,该反应的反应类型是 ;
②已知硝基苯在过量的Fe粉和盐酸的作用下可制得苯胺,写出该反应的化学方程式 .
查看习题详情和答案>>
 )等污染物的废水流入松花江,最终经俄罗斯入海.
)等污染物的废水流入松花江,最终经俄罗斯入海.(1)写出上述四种污染物中含有的官能团的结构简式
(2)苯、甲苯、硝基苯和苯胺4种物质的关系为
A.同系物 B.同分异构体 C.芳香烃 D.芳香族化合物
(3)苯胺和NH3与酸反应的性质相似,写出苯胺与盐酸反应的离子方程式
(4)①写出由苯制硝基苯的化学方程式
②已知硝基苯在过量的Fe粉和盐酸的作用下可制得苯胺,写出该反应的化学方程式
[化学-选修/物质结构与性质]
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于 .
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为 .
(2)下表为元素周期表的一部分,根据此表回答下列问题:
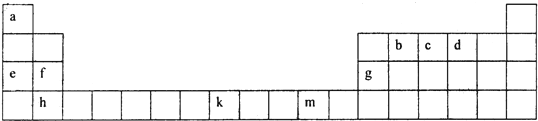
①f、g、h三种元素的第一电离能由小到大的顺序是 (用元素符号表示),b、c、d三种元素的电负性由大到小的顺序是 (用元素符号表示),b、c、d分别与a形成的简单化合物分子中,属于含有极性键的非极性分子是 .(填写化学式)
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式 .
目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为 .
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
,其中各原子的最外层电子均满足8电子稳定结构.该阴离子的中心原子的杂化轨道方式为 杂化,阴离子的电子式为 .
查看习题详情和答案>>
(1)①对硝基苯酚水合物(2C6H5NO3?3H2O)晶体属于分子晶体,实验表明,加热至94℃时该晶体失去结晶水,该晶体失去结晶水的过程,破坏的微粒间的主要作用力属于
②一种铜与金形成的合金,其晶体具有面心立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子的数目之比为
(2)下表为元素周期表的一部分,根据此表回答下列问题:

①f、g、h三种元素的第一电离能由小到大的顺序是
②有一种元素x和上表中所列元素k位于同周期、同一族且不相邻的位置,请写出元素x原子的基态价电子排布式

目前,利用金属或合金作为储氢材料的研究取得很大进展,如图是一种La-x合金储氢后的晶胞结构图.该合金储氢后,含有lmol La(镧)的合金中吸附的H2的数目为
③科学家把由c、d、e组成的离子化合物ecd 3和e2d在一定条件下反应得到一种白色晶体,该晶体中的阴离子为cd
3- 4 |
下列说法正确的是( )
| A、酒精中是否含有水,可用金属钠检验 | B、除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏 | C、分子式为C4H10O并能与金属钠反应放出氢气的有机化合物有3种 | D、用苯萃取溴水中的溴,分液时有机层从分液漏斗的下端放出 |
(2013?闵行区二模)氟化硅(SiF4)是有毒的无色气体,可用于水泥和人造大理石的硬化剂等,制取氟化硅
(SiF4)的化学方程式:2CaF2+H2SO4+SiO2
CaSO4+SiF4↑+H2O,完成下列填空:
(1)CaF2又名“萤石”,属于
 .
.
(2)不能用于比较F与O这两种元素非金属性强弱的事实是
a.F2能与H2O反应 b.H2O的沸点比HF高
c.HF的分解温度比H2O高 d.存在OF2化合物
(3)反应物中有三种元素在元素周期表中处于相邻,比较三种元素简单离子的半径由大到小顺序为
(4)已知SiF4的沸点为-65℃,则SiCl4的沸点
查看习题详情和答案>>
(SiF4)的化学方程式:2CaF2+H2SO4+SiO2
| △ |
(1)CaF2又名“萤石”,属于
离子
离子
晶体.在上述反应的反应物和生成物中,属于非极性分子的结构式

(2)不能用于比较F与O这两种元素非金属性强弱的事实是
b
b
(选填编号).a.F2能与H2O反应 b.H2O的沸点比HF高
c.HF的分解温度比H2O高 d.存在OF2化合物
(3)反应物中有三种元素在元素周期表中处于相邻,比较三种元素简单离子的半径由大到小顺序为
S2->O2->F-
S2->O2->F-
(用离子符号表示),其中离子半径最大的离子电子排布式为1s22s22p63s23p6
1s22s22p63s23p6
.(4)已知SiF4的沸点为-65℃,则SiCl4的沸点
高
高
(填“高”或“低”)于-65℃,其原因是:SiF4与SiCl4同属分子晶体且组成与结构相似,SiCl4的相对分子质量大,分子间作用力大,所以其沸点高于SiF4
SiF4与SiCl4同属分子晶体且组成与结构相似,SiCl4的相对分子质量大,分子间作用力大,所以其沸点高于SiF4
.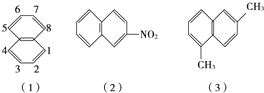 苯环上的碳原子的编号如(1)式,根据系统命名法,(2)式可称为2硝基萘,则化合物(3)的名称应是( )
苯环上的碳原子的编号如(1)式,根据系统命名法,(2)式可称为2硝基萘,则化合物(3)的名称应是( )