摘要:23.答案:(1)CaCO3+2HCl=CaCl2+H2O+CO2↑ (2)B 饱和NaHCO3 除CO2中的HCl C Na2O2粉末 反应物 D NaOH溶液 除去未反应的CO2 (3)2Na2O2+2CO2=2Na2CO3+O2 (4)将带火星的木条插入试管检验木条能否复燃. 解析:要证明过氧化钠可作供氧剂.必须验证实验产物是O2.故实验目的就是验证过氧化钠与水或二氧化碳的反应.实验仪器中的A是二氧化碳发生装置.B.D是除杂装置.C是反应装置.E是尾气处理与收集装置.本实验可能存在的杂质气体有:HCl和水.但由于过氧化钠与二氧化碳的反应是离子反应.故水不必除去.试管F中收集满气体后.下一步实验操作应是验证实验产物是O2.为检验生成的O2应将试管F从水槽中取出.然后用带火星的木条伸入管口进行检验.但是取出F前.应将装置A中的反应停止.
网址:http://m.1010jiajiao.com/timu3_id_413345[举报]
从A.甲醛 B.葡萄糖 C.乙醇 D.乙酸 E.油脂 等五种有机物中选择合适的答案,将其标号填在空格内.
(1)工业上制备肥皂的主要原料是
(2)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是
(3)家居装修材料中散发出的有毒物质是
(4)常用做燃料和医药上消毒剂的是
(5)糖尿病人通常是指病人的尿液中
查看习题详情和答案>>
(1)工业上制备肥皂的主要原料是
E
E
.(2)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是
D
D
.(3)家居装修材料中散发出的有毒物质是
A
A
(4)常用做燃料和医药上消毒剂的是
C
C
(5)糖尿病人通常是指病人的尿液中
B
B
的含量高.(2011?闵行区二模)天然水由于长期与土壤、岩石等接触,会溶有一定量的Ca2+、Mg2+、HCO3-等,这样的水在加热过程中很容易形成水垢.水垢可以看作由多种物质如:CaCO3、MgCO3、Mg(OH)2等中的若干种物质组成的混合物,某学习小组为研究含有Ca2+、Mg2+、HCO3-的自来水所形成水垢的化学组成,取干燥的水垢6.32g,加热使其失去结晶水后,得到5.78g剩余固体A;高温灼烧A至恒重,残余固体为CaO和MgO,放出的气体用足量Ba(OH)2溶液吸收,得到11.82g沉淀.
(1)通过计算确定A中的碳酸盐是
a.只有CaCO3 b.只有MgCO3 c.既有CaCO3又有MgCO3
写出计算过程:
(2)5.78g剩余固体A灼烧至恒重时产生的气体完全被碱石灰吸收,碱石灰增重2.82g,通过计算确定A中各成分的物质的量.若用a CaCO3?b MgCO3?x Mg(OH)2?y H2O表示原水垢(若a、b、x、y中有为0的,则该项略去,a、b、x、y用最简整数比),通过计算确定原水垢的化学式.
(3)该学习小组用该水垢模拟石灰窑反应,取该水垢与碳粉混合,通入一定量空气(假定不考虑其它气体,N2与O2体积比为:4:1),在密闭容器中,用喷灯加热至1000℃左右充分反应后,冷却到室温,测得最后所得气体中各种成分的体积含量如下:
O2:0.3%;CO:0.4%;CO2:42.5%;其余为N2.[已知:Mg(OH)2分解温度为270℃左右,MgCO3分解温度为400℃左右,CaCO3分解温度900℃左右].
求该小组所取水垢和碳粉的质量比(结果保留2位小数).
查看习题详情和答案>>
(1)通过计算确定A中的碳酸盐是
c
c
(填答案编号).a.只有CaCO3 b.只有MgCO3 c.既有CaCO3又有MgCO3
写出计算过程:
n(CO2)=n(BaCO3)=
=0.06mol,假设二氧化碳全部来自碳酸钙,则m(CaCO3)=0.06mol×100g/mol=6g>5.78g,假设二氧化碳全部来自碳酸镁,则m(MgCO3)=0.06mol×84g/mol=5.04g<5.78g,故A既含有CaCO3,又含有MgCO3
| 11.82g |
| 197g/mol |
n(CO2)=n(BaCO3)=
=0.06mol,假设二氧化碳全部来自碳酸钙,则m(CaCO3)=0.06mol×100g/mol=6g>5.78g,假设二氧化碳全部来自碳酸镁,则m(MgCO3)=0.06mol×84g/mol=5.04g<5.78g,故A既含有CaCO3,又含有MgCO3
| 11.82g |
| 197g/mol |
(2)5.78g剩余固体A灼烧至恒重时产生的气体完全被碱石灰吸收,碱石灰增重2.82g,通过计算确定A中各成分的物质的量.若用a CaCO3?b MgCO3?x Mg(OH)2?y H2O表示原水垢(若a、b、x、y中有为0的,则该项略去,a、b、x、y用最简整数比),通过计算确定原水垢的化学式.
(3)该学习小组用该水垢模拟石灰窑反应,取该水垢与碳粉混合,通入一定量空气(假定不考虑其它气体,N2与O2体积比为:4:1),在密闭容器中,用喷灯加热至1000℃左右充分反应后,冷却到室温,测得最后所得气体中各种成分的体积含量如下:
O2:0.3%;CO:0.4%;CO2:42.5%;其余为N2.[已知:Mg(OH)2分解温度为270℃左右,MgCO3分解温度为400℃左右,CaCO3分解温度900℃左右].
求该小组所取水垢和碳粉的质量比(结果保留2位小数).
 某化学兴趣小组的学生从网上查得如下信息:①钠能在CO2中燃烧.②常温下CO能与PdCl2溶液反应得到黑色的Pd.经过分析讨论,他们认为钠在CO2中燃烧时,还原产物可能是碳,也可能是CO,氧化产物可能是Na2CO3.为验证上述推断,他们设计如下方案进行实验,请回答下列问题.
某化学兴趣小组的学生从网上查得如下信息:①钠能在CO2中燃烧.②常温下CO能与PdCl2溶液反应得到黑色的Pd.经过分析讨论,他们认为钠在CO2中燃烧时,还原产物可能是碳,也可能是CO,氧化产物可能是Na2CO3.为验证上述推断,他们设计如下方案进行实验,请回答下列问题.(1)他们欲用上述装置组装一套新装置:用石灰石与盐酸反应制取CO2(能随意控制反应的进行)来证明钠能在CO2中燃烧并检验其还原产物,所用装置接口连接顺序为
jcdabefg(e与f可颠倒)
jcdabefg(e与f可颠倒)
,制取CO2反应的离子方程式为CaCO3+2H+═Ca2++H2O+CO2↑
CaCO3+2H+═Ca2++H2O+CO2↑
.(2)装置连接好后,首先要进行的实验操作是
检查装置的气密性
检查装置的气密性
,点燃酒精灯前,应进行的操作是打开F中导管上的止水夹
打开F中导管上的止水夹
,等装置D中澄清石灰水变浑浊
D中澄清石灰水变浑浊
(填写装置字母代号及现象)时,再点燃酒精灯,这步操作的目的是排尽装置内的空气
排尽装置内的空气
.(3)若装置D的PdCl2溶液中有黑色沉淀,C中有残留固体(只有一种物质),则C中反应的化学方程式为
2Na+2CO2═Na2CO3+CO
2Na+2CO2═Na2CO3+CO
;若装置D的PdCl2溶液中无黑色沉淀,C中有残留固体(有两种物质),则C中反应的化学方程式为
4Na+3CO2═2Na2CO3+C
4Na+3CO2═2Na2CO3+C
.(4)后来有一位同学提出,钠的氧化产物也可能是Na2O,因此要最终确定钠的氧化产物是何种物质,还需要检验C中残留的固体是否含有Na2O,为此,他认为应较长时间通入CO2以确保钠反应完,然后按照如下方案进行实验,可确定残留固体中是否含有Na2O,他的实验方案是
将残留固体溶于水,在所得水溶液中加入过量BaCl2溶液,再向溶液中滴加2滴酚酞试液,若溶液变红色,则残留固体中含有Na2O,否则不含Na2O(其他合理答案也可)
将残留固体溶于水,在所得水溶液中加入过量BaCl2溶液,再向溶液中滴加2滴酚酞试液,若溶液变红色,则残留固体中含有Na2O,否则不含Na2O(其他合理答案也可)
.从下面的六种有机物中选择合适的答案,将其标号填在空格内.
A.甲烷 B.甲醛 C.油脂 D.乙醇 E.乙酸 F.葡萄糖
(1)医疗消毒常用75%(体积分数)的 .
(2)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是 .
(3)最简单的有机物是 .
(4)工业上制备肥皂的主要原料是 .
(5)糖尿病患者的尿液中含有 ,该物质的溶液与新制Cu(OH)2悬浊液共热,产生 (填“蓝色”或“砖红色”)沉淀.
查看习题详情和答案>>
A.甲烷 B.甲醛 C.油脂 D.乙醇 E.乙酸 F.葡萄糖
(1)医疗消毒常用75%(体积分数)的
(2)能用于除去热水瓶胆水垢〔主要成分:CaCO3,Mg(OH)2〕的是
(3)最简单的有机物是
(4)工业上制备肥皂的主要原料是
(5)糖尿病患者的尿液中含有
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量)
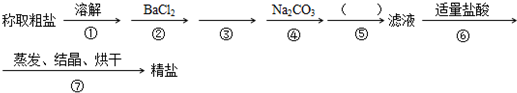
(1)判断BaCl2已过量的方法是
(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
(3)在 中 填写所使用除杂试剂的化学式
中 填写所使用除杂试剂的化学式
(4)从实验设计方案优化的角度分析步骤②和④可否颠倒
(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:
查看习题详情和答案>>

(1)判断BaCl2已过量的方法是
取第②步后的上层清液1~2滴于点滴板上(或取少量上层清液于试管中),再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(合理答案皆可)
取第②步后的上层清液1~2滴于点滴板上(或取少量上层清液于试管中),再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量(合理答案皆可)
.(2)第④步中,写出相应的化学方程式(设粗盐溶液中Ca2+的主要存在形式为CaCl2)
CaCl2+Na2CO3=CaCO3↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl
CaCl2+Na2CO3=CaCO3↓+2NaCl、BaCl2+Na2CO3=BaCO3↓+2NaCl
.(3)在
 中 填写所使用除杂试剂的化学式
中 填写所使用除杂试剂的化学式NaOH
NaOH
,在 ( )中的操作名称是过滤
过滤
.(4)从实验设计方案优化的角度分析步骤②和④可否颠倒
否
否
(填“是”或“否”,如果“否”,请说明理由.)原因是:过量的BaCl2必须要用Na2CO3除去,步骤复杂
过量的BaCl2必须要用Na2CO3除去,步骤复杂
;步骤③和④可否颠倒是
是
.(5)若先用盐酸再进行操作⑤,将对实验结果产生影响,其原因是:
会有部分沉淀溶解,从而影响制得精盐的纯度
会有部分沉淀溶解,从而影响制得精盐的纯度
.