网址:http://m.1010jiajiao.com/timu3_id_413338[举报]
(12分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇的反应为:CO(g)+2H2(g)CH3OH(g);ΔH
(1)已知,该反应在300℃,5MPa条件下能自发进行,则ΔH 0,△S 0 (填“<,>或=”)。
(2)在300℃,5MPa条件下,将0.20mol的 CO与0.58mol H2的混合气体充入2L密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。
①在0~2min内,以H2表示的平均反应速率为 mol·L-1·s-1。
②列式计算300℃时该反应的平衡常数K = 。
③300℃时,将0.50mol CO、1.00mol H2和1.00 molCH3OH充入容积为2L的密闭容器中,此时反应将 。
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
④下列措施可增加甲醇产率的是
A.压缩容器体积 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它条件不变,使反应在500℃下进行,在图中作出甲醇的物质的量浓度随时间的变化的示意图。
【解析】(1)根据反应的特点可知△S小于0,因为反应在300℃,5MPa条件下能自发进行,所以根据△G=△H-T·△S可知反应是放热反应。
(2)①反应速率通常用单位时间内浓度的变化量来表示,根据图像可知反应进行到2min时甲醇
的浓度不再发生变化,平衡时甲醇的物质的量是0.04mol,则消耗氢气是0.08mol,所以在0~2min
内,以H2表示的平均反应速率为![]() 。
。
②平衡时氢气的浓度是![]() ,CO的平衡浓度是
,CO的平衡浓度是
![]() ,所以该温度下的平衡常数为
,所以该温度下的平衡常数为![]() 。
。
③300℃时,将0.50mol CO、1.00mol H2和1.00 molCH3OH充入容积为2L的密闭容器中,此时它们的浓度分别为0.25mol/L、0.50mol/L、、0.50mol/L,因为![]() >4,所以反应向逆反应方向移动。
>4,所以反应向逆反应方向移动。
④压缩体积,压强增大,平衡向正反应方向移动。选项B是降低生成物浓度,平衡也向正反应方
向移动。充入He,使体系总压强增大,但物质但浓度没有变化,所以平衡不移动。再充入0.20mol
CO和0.58mol H2,相当于增大体系的压强,平衡向正反应方向移动,所以答案是ABD。
(3)因为反应是放热反应,所以升高温度平衡向逆反应方向移动,但反应速率会加快,所以图
像为
查看习题详情和答案>>
(12分)能源短缺是人类社会面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g);ΔH
CH3OH(g);ΔH
(1)已知,该反应在300℃,5MPa条件下能自发进行,则ΔH 0,△S 0 (填“<,>或=”)。
(2)在300℃,5MPa条件下,将0.20mol的 CO与0.58mol H2的混合气体充入2L密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示。

①在0~2min内,以H2表示的平均反应速率为 mol·L-1·s-1 。
②列式计算300℃时该反应的平衡常数K = 。
③300℃时,将0.50mol CO、1.00mol H2和1.00 mol CH3OH充入容积为2L的密闭容器中,此时反应将 。
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
④下列措施可增加甲醇产率的是
A.压缩容器体积 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.再充入0.20mol CO和0.58mol H2
(3)若其它条件不变,使反应在500℃下进行,在图中作出甲醇的物质的量浓度随时间的变化的示意图。
【解析】(1)根据反应的特点可知△S小于0,因为反应在300℃,5MPa条件下能自发进行,所以根据△G=△H-T·△S可知反应是放热反应。
(2)①反应速率通常用单位时间内浓度的变化量来表示,根据图像可知反应进行到2min时甲醇
的浓度不再发生变化,平衡时甲醇的物质的量是0.04mol,则消耗氢气是0.08mol,所以在0~2min
内,以H2表示的平均反应速率为 。
。
②平衡时氢气的浓度是 ,CO的平衡浓度是
,CO的平衡浓度是
 ,所以该温度下的平衡常数为
,所以该温度下的平衡常数为 。
。
③300℃时,将0.50mol CO、1.00mol H2和1.00 mol
CH3OH充入容积为2L的密闭容器中,此时它们的浓度分别为0.25mol/L、0.50mol/L、、0.50mol/L,因为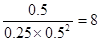 >4,所以反应向逆反应方向移动。
>4,所以反应向逆反应方向移动。
④压缩体积,压强增大,平衡向正反应方向移动。选项B是降低生成物浓度,平衡也向正反应方
向移动。充入He,使体系总压强增大,但物质但浓度没有变化,所以平衡不移动。再充入0.20mol
CO和0.58mol H2,相当于增大体系的压强,平衡向正反应方向移动,所以答案是ABD。
(3)因为反应是放热反应,所以升高温度平衡向逆反应方向移动,但反应速率会加快,所以图
像为

查看习题详情和答案>>
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g) △H <0,在673K、30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )
A、点 c处反应达到平衡
B、点a的正反应速率比点b的大
C、点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D、其他条件不变,773K下反应至t1时刻,n(H2)比图中d点的值小。
【解析】c点之后物质的量是变化的,所以c点没有达到平衡状态,A不正确。A点反应物的浓度减小,生成物的浓度增加,所以a点正反应速率大于逆反应速率,B正确。d和e均是相同条件下的平衡状态,所以氮气的物质的量是相同的,C不正确。因为反应是放热反应,所以温度升高,平衡向逆反应方向移动,氢气的物质的量是增加的,因此D也是错误的。答案选B。
查看习题详情和答案>>
合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)  2NH3(g) △H <0,在673K、30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )
2NH3(g) △H <0,在673K、30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是 ( )
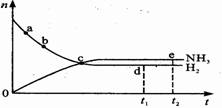
A、点 c处反应达到平衡
B、点a的正反应速率比点b的大
C、点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样
D、其他条件不变,773K下反应至t1时刻,n(H2)比图中d点的值小。
【解析】c点之后物质的量是变化的,所以c点没有达到平衡状态,A不正确。A点反应物的浓度减小,生成物的浓度增加,所以a点正反应速率大于逆反应速率,B正确。d和e均是相同条件下的平衡状态,所以氮气的物质的量是相同的,C不正确。因为反应是放热反应,所以温度升高,平衡向逆反应方向移动,氢气的物质的量是增加的,因此D也是错误的。答案选B。
查看习题详情和答案>>
(12分)某活动小组探究某无色晶体(纯净物)的组成。先测得相对分子质量为126;经元素分析可知:只含碳、氢、氧三种元素;该无色晶体受热能分解。然后设计了下列实验方案再对其进行定量分析:
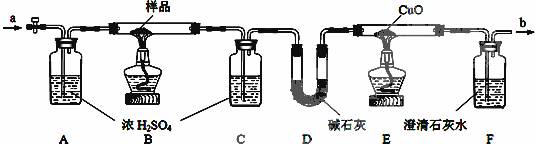
【实验操作】(1)检查装置的气密性;
(2)在相应的仪器中放入相应的试剂,并称量C、D、E的质量;
(3)先从a处通入足量的N2,排尽装置中的空气;
(4)点燃B、E两处的酒精灯,缓缓加热样品,使之发生分解反应;
(5)当样品完全分解后,先熄灭B处的酒精灯,从a处缓缓通入足量的N2,再熄灭E处酒精灯;
(6)冷至室温,拆下各仪器,并称量C、D、E的质量。
【实验现象】 ① E处有红色物质生成,F处有白色沉淀生成;
② 由于实验条件控制得好,b处无可燃性气体放出。
请回答下列问题:
(1)用最简便的方法检查整套装置的气密性:
。
(2)仪器A的作用是 。
(3)操作(3)和(5)若是通入空气,其后果是
。
(4)数据处理:
① 实验记录的数据(各仪器中的吸收或反应都很完全):
| 样品的质量 | C装置增重 | D装置增重 | E装置减轻 |
| 12.6 g | 5.4 g | 4.4 g | 1.6 g |
② 计算判断:样品(无色晶体)的分子式为______________________。
查看习题详情和答案>>