摘要:4.答案:AB 解析:与钠元素相似.铷元素也有焰色反应.选项A正确,与NaNO3相似.RbNO3是离子化合物.易溶于水.选项B正确,碱金属从锂到铯.熔点逐渐降低.选项C错误,碱金属的氢氧化物均为强碱.选项D错误.
网址:http://m.1010jiajiao.com/timu3_id_413326[举报]
钠的下列用途正确且与钠的化学性质无关的是( )??
①与钾形成的合金可作原子反应堆的导热剂
②制取Na2O2
③冶炼稀有金属及金属钛
④应用于电光源上
⑤制取NaOH及NaCl等钠的化合物
⑥可用于验证乙醇的分子结构.
①与钾形成的合金可作原子反应堆的导热剂
②制取Na2O2
③冶炼稀有金属及金属钛
④应用于电光源上
⑤制取NaOH及NaCl等钠的化合物
⑥可用于验证乙醇的分子结构.
查看习题详情和答案>>
某芳香族化合物的分子式为C7H8O,根据下列实验现象确定其结构简式:(要求:每小题只需给出一个答案即可.)
①不能与金属钠反应,其结构简式为
②能与钠反应,但遇FeCl3不显色
③能与钠反应且遇FeCl3显紫色 (或
(或 或
或 )
) (或
(或 或
或 ).
).
查看习题详情和答案>>
①不能与金属钠反应,其结构简式为
C6H5OCH3
C6H5OCH3
.②能与钠反应,但遇FeCl3不显色
C6H5CH2OH
C6H5CH2OH
.③能与钠反应且遇FeCl3显紫色
 (或
(或 或
或 )
) (或
(或 或
或 )
)有机物在反应中常有原子问的共价键全部或部分断裂,如C-H、C-C、C=C、C-0、C=O等.下列各反应中,反应物分子中断裂键的正确组合是( )
|
查看习题详情和答案>>
已知X,Y,Z,Q为短周期非金属元素,R是长周期元素,X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+离子只有三个电子层且完全充满电子。
回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)X元素为???????? ,X、Y、Z中第一电离能最大的是???????? 。
(2)已知Y2Q2分子存在如图所示的两种结构(球棍模型,短线不一定代表单键):
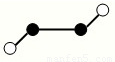
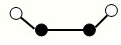
该分子中Y原子的杂化方式是???????? 。
(3)X与Y元素可以形成一种超硬新材料,其晶体部分结构如图所示,有关该晶体的说法正确的是???? (填正确答案编号)。

A.该晶体属于分子晶体
B.此晶体的硬度比金刚石还大
C.晶体的化学式是X3Y4
D.晶体熔化时破坏共价键
(4)有一种AB型分子与Y单质分子互为等电子体,它是一种常用的还原剂,其化学式为????????????? 。
(5)R的基态原子的电子排布式为????????? ,R与Z形成的某离子晶体的晶胞结构如图,则该晶体的化学式为????????? ,该晶体的密度为a g·cm-3,则晶胞的体积是????????? cm3。
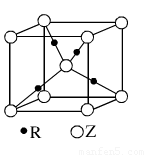
查看习题详情和答案>>